Симпато-адреналовые кризы (панические атаки)
Это неуправляемый, нерациональный, изматывающий и очень интенсивный приступ паники и тревоги, который сопровождается соматическими и психологическими симптомами. Состояние может воздействовать на когнитивные способности и поведенческие реакции.
Они довольно часто встречаются в популяции, примерно в 5% случаев и, что самое интересное, им подвержены молодые работоспособные граждане от 20 до 40 лет, причем женщины страдают этим недугом в 3 раза чаще.
Из-за огромного количества схожих симптомов врачи разных специальностей называют панические атаки по-разному , но в целом все эти названия являются синонимами и очень похожи (поэтому в тексте мы будем использовать все названия):
- Вегетативный криз
- Симпато-адреналовый криз
- Вегетососудистая дистония
- Нейроциркуляторная дистония
- Кардионевроз
Сразу
хочется отметить, что при адекватном,
начатом вовремя, а главное комплексном
лечении данной проблемы возможен  К сожалению, при отсутствии лечения,
болезнь может прогрессировать из редких,
нечастных приступов в хроническую
форму ,
при которой частота и сила приступов
постоянно возрастает и может перейти
в более серьезные
психические проблемы .
Поэтому мы советуем вам записаться на
прием к нашим специалистам – они очень
эффективно лечат панические атаки в
Усть-Каменогорске на базе центра Пульс.
К сожалению, при отсутствии лечения,
болезнь может прогрессировать из редких,
нечастных приступов в хроническую
форму ,
при которой частота и сила приступов
постоянно возрастает и может перейти
в более серьезные
психические проблемы .
Поэтому мы советуем вам записаться на
прием к нашим специалистам – они очень
эффективно лечат панические атаки в
Усть-Каменогорске на базе центра Пульс.
Перед тем, как переходить к проявлению заболевания, обратимся к небольшой классификации для лучшего понимания.
Выделяют 3 типа панических атак.
- Спонтанная паническая атака — самая неблагоприятная форма течения заболевания, когда пациент не может выделить четкого пускового фактора после которого начинается приступ, и соответственно не может к нему подготовиться.
- Ситуационная
паническая атака – имеет психо-соматические «корни»,
проявляется в какой-то определенной
психотравмирующей ситуации или в
ожидании такой ситуации.

- Условно-ситуационная атака – в данном случае к психологическому триггеру присоединяется химический или биологический. Например, употребление кофе, чая, алкогольных напитков, изменение гормонального фона и др.
Немного о симптомах и патогенезе заболевания.
Что именно происходит с организмом? От чего такие симптомы? Из-за чего это случилось? Именно такие вопросы задают себе пациенты и это не удивительно ! Ведь клиническая картина болезни может быть весьма запутана и разобраться в ней без помощи опытного специалиста очень трудно.
Приступы
носят ярко выраженный соматический,
т.е. телесный и физический характер, по
своим симптомам очень напоминающий
классический сердечный приступ
сопровождающийся страхом
смерти и пр. , поэтому пациенты могут предполагать
у себя патологию сердца (отсюда и одно
из названий – сердечный невроз). Однако,
даже самые сильные проявления атак,
следствие дисбаланса нервной и гуморальной
систем. Основным механизмом развития
криза является активация симпатической
нервной системы и мощный выброс
, поэтому пациенты могут предполагать
у себя патологию сердца (отсюда и одно
из названий – сердечный невроз). Однако,
даже самые сильные проявления атак,
следствие дисбаланса нервной и гуморальной
систем. Основным механизмом развития
криза является активация симпатической
нервной системы и мощный выброс
Как
мы уже говорили, для вегетативных кризов
характерно обилие резко возникающих
симптомов. В первую очередь это фобическая
тревога ,
т.е. неконтролируемый панический страх.
Так как происходит выброс адреналина,
учащается сердцебиение,
может появляться боль
в груди и области сердца, артериальное 
Так как часто вовлекается психика, то могут наблюдаться ее кратковременные расстройства: человеку кажется, что все это происходит не с ним, возникает ощущение нереальности происходящего, отчуждаются собственные психические процессы, появляется страх перестать контролировать свое поведение
Клиническая картина и ее выраженность имеет широкий диапазон и очень варьируется, существует даже так называемая « безстраховая» форма панической атаки или «паника без паники», когда на первый план выходят именно физические нарушения.
Так же, как и симптомы, изменчива длительность приступов. Они могут появляться на несколько минут, а могут длиться часами, но в среднем укладываются в 15 – 30 минут. Частота таких приступов тоже не имеет четкой зависимости: у кого-то это 1 раз в месяц, у кого-то 3 раза в день.
Такие
кризы, как правило, не
носят единичного характера.
Как таковые причины панических атак до конца не выяснены, вот некоторые из возможных:
- Нарушение системы кровообращения, в частности за счет вертебральных артерий и патологических процессов в шейном отделе позвоночника.
- Гормональный
дисбаланс, не редко с вовлечением
щитовидной железы.

- Хроническая соматическая патология, органические поражения центральной нервной системы, недавнее инфекционное заболевание.
- Стресс (положительный и отрицательный), пребывание в неблагоприятной обстановке (смерть близкого, частые ссоры в семье, рождение ребенка).
- Неправильное воспитание, детские страхи (чрезмерная требовательность и критичность со стороны родителей).
- Особенности функционирования психики, личностные особенности, темперамент.
- Генетическая предрасположенность.
Есть интересное мнение, что недугу чаще всего подвержены люди, живущие в городах, интеллектуально развитые, тревожные и ответственные от природы. Практически не встречаются люди с вегетативными кризами среди жителей отдаленных районов и деревень.
В
связи с многофакторностью причин
заболевания установить точную причину
и, соответственно, назначить правильное
лечение  Усть-Каменогорск
ул.Красина д1.
Усть-Каменогорск
ул.Красина д1.
Диагностика.
Данный
диагноз можно установить по следующим
объективным причинам: повторное
возникновение приступа с нарастанием
пика на 10-15 минуте и возникновением хотя
бы 4х из описанных выше симптомов. Но
диагностика не так проста ,
трудности заключаются в том, что
существует большое количество соматических
заболеваний со схожей клинической
картиной. Многие из них потенциально
Как осуществляется лечение панических атак в Усть-Каменогорске?
После
исключения прочих соматических патологий
и определения причинны заболевания
наступает черед лечения.
Для восстановления баланса процессов возбуждения и торможения в нервной системе используется иглорефлексотерапия, магнито- и лазеротерапия. Хорошие результаты в лечении панических атак дает транскраниальная стимуляция головного мозга.
Если причина связана с нарушением гемодинамики на уровне брахиоцефальных артерий, то применяется мануальная терапия, массаж, вытяжение позвоночника.
Совокупность
опыта наших врачей, умение правильно
оказать психотерапевтическую помощь,
большая база физиотерапевтических
аппаратов и знания рефлексотерапии
позволяется с
успехом лечить панические атаки в центре
Пульс . В нашей клинике любого пациента поймут,
поддержат и обязательно помогут.
Записывайтесь на прием по телефону 8-7
В нашей клинике любого пациента поймут,
поддержат и обязательно помогут.
Записывайтесь на прием по телефону 8-7
причины, симптомы и лечение заболевания
Вегетативный криз — это пароксизмальное состояние человека, носящее неэпилептический характер. Он проявляется полиморфным вегетативным расстройством, которое наступает вследствие активизации центральной или, иначе говоря, подсегментарной вегетативной структуры. Во время криза проявляются все симптомы синдрома вегетативной дисфункции, имеющие наиболее яркие и выраженные проявления. Для этого заболевания характерны мучительные приступы необъяснимой тревоги и непонятного страха, которые сопровождают различные симптомы соматического порядка.
Классификация
У вегетативного криза нет единой классификации. Его обычно подразделяют на типы, которые имеют различную степень тяжести и симптомы, связанные в свою очередь, с показаниями артериального давления и работой сердечно-сосудистой системы.
Вегетативный криз делится на несколько типов с разной степенью тяжести. Для легкого характерны непродолжительные приступы по 10-15 мин, с ярко выраженными нарушениями со стороны вегетативной системы и проявлениями моносимптомного характера, при этом нет посткризовой астении. Приступы средней тяжести могут длиться от 15-20 мин до часа, при этом присутствуют полисимптомные проявления и посткризовая астения, которые продолжаются в течении 24-36 часов. Во время тяжелого приступа наблюдается комбинация полисимптомных кризов вместе с судорогами и гиперкинезами, это состояние длится больше одного часа и сопровождается многодневной астенией.
Вегетативный криз по симптоматике подразделяют на: вагоинсулярный, симпатоадреналовый и смешанный.
Симптомы
Вегетативный криз чаще всего первый раз проявляется в определенном возрасте — в основном это 20-30 лет. Но были отмечены случаи диагностирования заболевания у детей до 15 лет и пожилых людей после 65. Основная категория людей, подвергающаяся приступам вегетативного криза — женщины. У мужчин это заболевание диагностируют в 2-3 раза реже, чем у представительниц слабого пола. Во время приступов панической атаки обычно вырисовывается следующая клиническая картина: ⅔ всех симптомов приходится на вегетативные, остальные — это эмоционально-аффективные расстройства. У каждого вида вегетативного криза свои симптомы, они зависят от степени тяжести панического расстройства и определяются при помощи специальной шкалы.
Основная категория людей, подвергающаяся приступам вегетативного криза — женщины. У мужчин это заболевание диагностируют в 2-3 раза реже, чем у представительниц слабого пола. Во время приступов панической атаки обычно вырисовывается следующая клиническая картина: ⅔ всех симптомов приходится на вегетативные, остальные — это эмоционально-аффективные расстройства. У каждого вида вегетативного криза свои симптомы, они зависят от степени тяжести панического расстройства и определяются при помощи специальной шкалы.
Для симпатоадреналового криза характерны следующие симптомы: нарушение работы сердца и учащенное сердцебиение, боли и пульсация в голове, повышенная температура, побледнение кожи, озноб, необъяснимое чувство страха. Заканчивается он внезапно, при этом выделяется большое количества мочи. После этого начинает развиваться астеническое состояние.
Симптомы вагоинсулярного криза выглядят следующим образом: человек начинает чувствовать нехватку воздуха, у него появляется чувство удушья, одышка, пульс становится редким, сердце работает с перебоями, кожа становится гиперемированной, появляется боль в желудке, усиливается перистальтика кишечника и пр.
В смешанном типе вегетативного криза сочетаются признаки видов, описанных ранее, т.е. симпатоадреналового и вагоинсулярного типов. Основными симптомами вегетативного криза данного типа являются приступы беспричинной паники, тревоги или страха, к которым добавляются несколько проявлений того или иного заболевания. Психосоматика человека в этом случае выдает такие ощущения, как деперсонализация, дереализация, возникает боязнь неконтролируемых поступков, потери разума, появляется страх смерти.
К наступлению вегетативного криза человека могут привести разные причины. Он может стать следствием длительного стресса или невроза, послеродовой травмы, травмы головы. Вызвать вегетативный криз могут и нарушения в работе центральной нервной системы, и такие состояния, как предменструальный синдром у женщин, мочекаменная болезнь, половое созревание и пр. Неконтролируемый прием каких либо лекарственных препаратов тоже может спровоцировать это заболевание.
Диагностика и лечение
Особых сложностей диагностика вегетативного криза в современной медицине не вызывает. Самое главное — это исключить серьезные заболевания психического, соматического или эндокринного плана.
Самое главное — это исключить серьезные заболевания психического, соматического или эндокринного плана.
У вегетативного кризиса существует три критерия диагностирования:
- Ограниченность во времени и приступообразный характер
- Наличие полисистемных расстройств вегетативной системы
- Наличие состояний эмоционально-аффективного характера
Современная медицина для лечения вегетативного криза использует мероприятия самого различного плана: психотерапевтические, фармакологические и психосоциальные. Самым лучшим и эффективным способом лечения этого заболевания считается прием психотропных препаратов вкупе с сеансами психотерапии.
Последствия и прогнозы
Если приступы вегетативного криза своевременно не купировать, то последствия могут быть весьма плачевными и тяжелыми. Память пациента надолго фиксирует пережитый приступ, и человек начинает со страхом ожидать повторения(так называемый”синдром ожидания”). Больной начинает избегать потенциально опасных для себя мест, и тех ситуаций, которые чреваты приступом. Это приводит к изменению в его поведении, нарушению психики, формированию фобий. В том случае, если человек вовремя обратится за помощью, прогнозы весьма положительные. Грамотное и адекватное лечение вегетативного криза не допустит повторения приступов, а, следовательно, и наступления серьезных последствий.
Больной начинает избегать потенциально опасных для себя мест, и тех ситуаций, которые чреваты приступом. Это приводит к изменению в его поведении, нарушению психики, формированию фобий. В том случае, если человек вовремя обратится за помощью, прогнозы весьма положительные. Грамотное и адекватное лечение вегетативного криза не допустит повторения приступов, а, следовательно, и наступления серьезных последствий.
Прием врача невролога первичный: 1850 Р.
Симпатоадреналовый Криз | Паническая Атака
В этой статье:
Симпатоадреналовый криз имеет несколько тождественных названий: вегетативно-сосудистый криз, церебральный вегетативный криз, паническая атака, вегетативная буря, вегетативные припадки, вегетативные кризы и др.
Международная классификация болезней МКБ-10
Согласно классификации МКБ-10, симпатоадреналовый криз классифицируется, как «рецидивирующие приступы резко выраженной тревоги (паники), которые не ограничены какой-либо особой ситуацией или комплексом обстоятельств и, следовательно, непредсказуемы».
Симптомы симпатоадреналового криза
Главные симптом симпатоадреналового криза – это приступы страха, накатывающие лавинообразно. Страх немотивированный, беспричинный с бурными эмоциональными реакциями и со сменой поведения. Паника сопровождается безотчетной тревогой, парализует страх смерти. Внутреннее напряжение сопровождается чувством надвигающейся беды. Но не только. Возникают и другие диенцефальные расстройства.
Симпатоадреналовый криз зависит от состояния функционального состояния диенцефальный области мозга
Неврологические проявления при симпатоадреналовом кризе касаются исключительно вегетативного отдела нервной системы. Центральное представительство всех вегетативных функций расположено в диенцефальной области мозга. Поэтому симпатоадреналовый криз называют диенцефальным кризом. Диенцефальная (промежуточная) область мозга (см. рисунок ниже) – это концентрация всех вегетативных неврологических представительств организма. Вегетативная – означает автономная, на зависимая от сознания. Ею практически невозможно управлять. Тем более, что эта зона мозга очень чувствительна к изменениям кровотока.
Вегетативная – означает автономная, на зависимая от сознания. Ею практически невозможно управлять. Тем более, что эта зона мозга очень чувствительна к изменениям кровотока.
Диенцефальный отдел мозга имеет прямую связь с гипофизом, который в свою очередь связан с надпочечниками. Надпочечники – единственный в организме орган, который синтезирует стрессовые гормоны.
При симпатоадреналовом кризе возбуждается диенцефальная область мозга, активирует гипофиз, который, в свою очередь, дает команду надпочечникам. Надпочечники выбрасывают в кровь адреналин, провоцируя адреналовый криз. Отсюда такой поток стрессовых реакций эмоциональных и вегетативных реакций.
Диенцефалный (симпатоадреналовый) криз. Неврологические симптомы
Неврологические расстройства при симпатоадреналовом кризе носят вегетативный характер. Вегетативные проявления следующие.
Симпатоадреналовый криз длится от 20 минут до нескольких часов и проявляется в виде немотивированного нарастающего страха в сочетании с вегетативными расстройствами (вегетативная буря). Вегетативные расстройства захватывают практически все отдела симпатической нервной системы, ощутимо меняется поведение. Для такого криза характерна беспричинная тревога, замирание сердца, страх смерти, необоснованное предчувствие беды.
Вегетативные расстройства захватывают практически все отдела симпатической нервной системы, ощутимо меняется поведение. Для такого криза характерна беспричинная тревога, замирание сердца, страх смерти, необоснованное предчувствие беды.
Характерны одышка, затруднение дыхания, чувство нехватки воздуха, тахикардия или брадикардия, боли в области сердца, которые заставляют думать об инфаркте миокарда, это усиливает стресс. Приступы ярости.
Может иметь место дискомфорт в верхней части живота (литературное – «тянет под ложечкой»). Может возникать отрыжка, жар или озноб, дрожь. Симпатоадреналовый криз проявляется сосудистыми реакциями со стороны головного мозга — головокружение, головная боль, шум в ушах, онемение или «ползание мурашек» (парестезии) в конечностях, онемение языка, губ. Нередко такой приступ оканчивается обильным мочеиспусканием или диареей.
В зависимости от того, какая области гипоталамуса более задействована, различают симпатоадреналовый и вагоинсулярный (парасимпатический) криз. Такое разделение условно, поскольку при анализе проявлений симпатоадреналового криза оказывается, что имеются проявления со стороны как симпатического, так и парасимпатического отделов нервной – смешанный криз. К симпатоадреналовым кризам склонны лица с неврозами. Хотя, сами неврозы – это исходные отклонения в эмоциональной сфере, обусловленные с диэнцефальной (гипоталамической) областью.
Такое разделение условно, поскольку при анализе проявлений симпатоадреналового криза оказывается, что имеются проявления со стороны как симпатического, так и парасимпатического отделов нервной – смешанный криз. К симпатоадреналовым кризам склонны лица с неврозами. Хотя, сами неврозы – это исходные отклонения в эмоциональной сфере, обусловленные с диэнцефальной (гипоталамической) областью.
Криз может провоцироваться стрессом, даже минимальным; неудовлетворенностью чем-либо, иными психогенными факторами. Кризы возникают при изменении эндокринного баланса, особенно у женщин с гормональными перестройками в пременопаузе и при климаксе. Эти кризы более похожи на вагоинсулярные.
Исходные гипоталамо-эндокринные расстройства обостряются при менструации, беременности, лактации… Криз нередко провоцируется некоторыми видами физической нагрузки, особенно интенсивными с повышением внутричерепного давления.
Вегетативные кризы в виде синдрома гипервозбудимости свойственны и детям с функциональными расстройствами центральной нервной системы, последствиями родовой авмы.
Лечение симпатоадреналовых кризов
Исследования, проведенные в Институте Неврологии и Мышечно-скелетной медицины, показали, что у людей, склонных вегетативным кризам имеются характерные отклонения мозгового кровотока. При этом нередко диагностируются некоторые особенности строения головного мозга. Также был определен пул ядер диэнцефальной области, воздействие на которые при симпатоадреналовых кризах приводило к стойкой ремиссии. Определенные МРТ технологии позволяют выявить некоторые изменения в области гипофиза, которые являются характерными для лиц с симпатоадреналовыми кризами и паническими атаками.
Для лечения симпатоадренаовых кризов используют не только медикаменты, но и т.н. вегетотропные методы. Учитывая то, что симпатоадреналовые и вагоинсулярные кризы возникают при патологии гипоталамуса, одним из таких методов является иглотерапия. Метод, способный нормализовать вегетативные функции гипоталамуса.
Следует отметить, что классическая китайская иглотерапия в большинстве случаев справляется с проблемой. Но, при условии адекватной коррекции кровотока и ликворотока в области гипоталамуса и гипофиза (диенцефальная область мозга).
Но, при условии адекватной коррекции кровотока и ликворотока в области гипоталамуса и гипофиза (диенцефальная область мозга).
Читать больше о гипоталамусе
Подобные вегетативные бури прослеживались нами при посттравматических стрессовых расстройствах (ПТСР). По своей направленности и клиническим проявлениям чаще их можно характеризовать, как затянувшийся устойчивый стресс с эпизодами «панических атак».
Оборудование, которое мы используем для диагностики
любой неврологической и ортопедической патологии, включая
вегетососудистую дистонию, симпатоадреналовые кризы, панические атаки и др.
МРТ аппарат Toshiba Vantage Elan 1.5 тесла
МРТ открытого типа Hitachi 0.4 тесла
УЗИ аппарат Philips AFFINITY 50
Цифровой рентген «Radspeed» SHIMADZU
доктор медицинских наук В.В.Гонгальский
Симпатоадреналовый криз Википедия
Пани́ческое расстро́йство, или эпизоди́ческая пароксизма́льная трево́га, — психическое расстройство, характеризующееся спонтанным возникновением панических атак от нескольких раз в год до нескольких раз в день и ожиданием их возникновения. Характерной чертой расстройства являются приступы резко выраженной тревоги (паники), которые не ограничены определённой ситуацией или обстоятельствами и, следовательно, непредсказуемы[1].
Характерной чертой расстройства являются приступы резко выраженной тревоги (паники), которые не ограничены определённой ситуацией или обстоятельствами и, следовательно, непредсказуемы[1].
Другие названия этого заболевания — «эпизодическая пароксизмальная тревожность, «кардионевроз», «ВСД (вегетососудистая дистония)» с кризовым течением», «НЦД (нейроциркуляторная дистония)»[2].
При панических атаках могут иметь место учащённое сердцебиение, боль в груди, затруднённое дыхание, мышечные спазмы, головокружение, тошнота. Иногда может появиться чувство нереальности происходящего (дереализация) и отстранённости от собственного тела (деперсонализация — ощущение нахождения вне тела и наблюдения за происходящим со стороны). Симптомы при атаке не поддаются контролю, это сильно деморализует человека, вызывает чувство бессилия и отчаяния[2]. Стремление человека сознательно контролировать своё состояние во время панической атаки делает симптомы еще более интенсивными[3]. Часто ожидание возможной атаки более мучительно, чем сама атака. Человек заранее боится, что он не справится с паникой или не сможет получить помощь. По этой причине многие больные начинают избегать ситуаций, в которых может возникнуть атака (например, остаться одному или выйти из дома)[2].
Часто ожидание возможной атаки более мучительно, чем сама атака. Человек заранее боится, что он не справится с паникой или не сможет получить помощь. По этой причине многие больные начинают избегать ситуаций, в которых может возникнуть атака (например, остаться одному или выйти из дома)[2].
Клиническая картина и диагностические критерии
У страдающих паническим расстройством людей, как правило, наблюдаются серии интенсивных эпизодов крайней (и, как правило, необъяснимой) тревоги — панических атак. Панические атаки обычно продолжаются около 10 минут, но могут быть и кратковременными — около 1—5 минут, и длительными — до 30 мин, при этом ощущение тревоги может сохраняться в течение 1 часа. Панические атаки могут различаться по набору симптомов или быть однотипными (то есть тахикардия, потливость, головокружение, одышка, тремор, переживание неконтролируемого страха и т. д.). У части пациентов данные состояния наблюдаются регулярно — иногда ежедневно или еженедельно. Внешние симптомы панической атаки часто ведут к негативным социальным последствиям (например, смущению, общественным порицаниям, социальной изоляции). Тем не менее, у знающих о своём заболевании пациентов часто могут быть интенсивные панические атаки с очень малыми внешними проявлениями этого состояния.
Внешние симптомы панической атаки часто ведут к негативным социальным последствиям (например, смущению, общественным порицаниям, социальной изоляции). Тем не менее, у знающих о своём заболевании пациентов часто могут быть интенсивные панические атаки с очень малыми внешними проявлениями этого состояния.
Для определения тяжести панического расстройства используется специальная шкала; она существует также в форме опросника самооценки в качестве теста на панические атаки[4][5].
Диагностические критерии МКБ-10
- Повторные, непредсказуемые приступы (не ограничивающиеся какой-либо определённой ситуацией) выраженной тревоги (паники).
- Сопровождающие тревогу вегетативные болевые симптомы, дереализация и деперсонализация.
- Вторичные страхи смерти и сумасшествия.
- Вторичное избегание какой-либо ситуации, в которой паническая атака возникла впервые.
- Вторичные страхи одиночества, людных мест, повторных панических атак.

- Паническое расстройство является основным диагнозом в случае отсутствия какой-либо фобии как первичного расстройства (в противном случае паническая атака рассматривается как признак выраженной фобии).
- Достоверный диагноз панического расстройства требует, чтобы несколько тяжёлых приступов тревоги наблюдалось по меньшей мере в течение одного месяца и отвечали следующим требованиям:
- Паническое расстройство возникает при обстоятельствах, не связанных с объективной угрозой (возможна тревога предвосхищения атаки).
- Паническое расстройство не ограничивается известной, предсказуемой ситуацией.
- Наличие свободных от тревоги периодов между атаками.
Диагностические критерии DSM-IV
- Повторяющиеся приступы панических атак.
- По крайней мере один приступ был в течение 1 месяца (или более) при следующих дополнительных симптомах:
- Сохраняющаяся обеспокоенность по поводу приступов.
- Беспокойство о последствиях приступа (например, страх утраты самоконтроля, инфаркта миокарда, страх сойти с ума).

- Значительные изменения в поведении, связанные с атаками.
- B. Присутствие (или отсутствие) агорафобии.
- C. Симптоматика не является последствием прямого физиологического воздействия вещества (например, злоупотребления наркотиками, лекарства) или какого-либо заболевания (например, артериальная гипертензия, гипертиреоз, феохромоцитома, и т. д.).
- Симптоматика не может быть объяснена наличием другого расстройства психики или поведения, такого как соматоформная вегетативная дисфункция сердца и сердечно-сосудистой системы, ипохондрия, социальная фобия, другие фобии, обсессивно-компульсивное расстройство, посттравматическое стрессовое расстройство или тревожное расстройство, вызванное разлукой.
Согласно диагностическому и статистическому руководству DSM-IV-TR панические атаки не рассматриваются как отдельное заболевание, а кодируются в составе диагноза других тревожных расстройств[6].
Дифференциальная диагностика
Паническое расстройство необходимо отличать от ряда соматических болезней и состояний, к которым относятся сердечно-сосудистые расстройства, хронические обструктивные болезни лёгких, некоторые эндокринные и метаболические расстройства (болезнь Кушинга, нарушения электролитного обмена, гипертиреоз, гипергликемия, заболевания паращитовидных желез), эпилепсия, в особенности височная; пептическая язва, феохромоцитома, лёгочная эмболия[7], , опухоли ЦНС, бронхиальная астма, эффекты некоторых лекарственных средств и наркотических веществ[8], состояния после сильных ожогов и обширных хирургических вмешательств.
Кроме того, паническое расстройство следует отличать от других психических расстройств, сопровождающихся паническими атаками: например, установленных фобических расстройств (F40.x), посттравматического стрессового расстройства, обсессивно-компульсивного расстройства, соматоформных расстройств (F4x.x) и других подобных нарушений. Панические атаки могут быть вторичными по отношению к депрессивным расстройствам тревожного спектра, особенно у мужчин, и если выявляются критерии депрессивного расстройства, то паническое расстройство не должно устанавливаться как основной диагноз.
Течение и распространённость
Паническое расстройство обычно начинается в молодом возрасте, реже в детском и зрелом. По результатам исследований, около 1,7 % взрослого населения США имели симптомы панического расстройства (женщины болеют чаще в 2—3 раза). Заболевание имеет волнообразное течение; около половины больных в целом выздоравливают, остальные ведут относительно нормальную жизнь, несмотря на сохранение симптоматики и наличие рецидивов.
Затяжному течению панического расстройства способствуют неадекватные и несвоевременные лечебные мероприятия. Тревожные расстройства, в том числе паническое, диагностируются лишь у 50 % пациентов с очевидными симптомами. Меньше чем 50 % пациентов получают какое-либо лечение и меньше 30 % — адекватную терапию.
Лечение
Несмотря на обязательное присутствие вегетативной дисфункции в приступе и часто неявный характер эмоциональных расстройств, основными методами лечения панического расстройства являются психотерапия и психофармакология.
Психофармакология
Используются антидепрессанты группы СИОЗС — длительно, не менее 6 месяцев; а также транквилизаторы (алпразолам, клоназепам) коротким курсом — до 14 дней.
На протяжении некоторого времени высокоактивные бензодиазепины, такие как алпразолам и клоназепам, считались препаратами первого выбора при лечении панического расстройства. Но отсутствие эффективности в отношении симптомов депрессии, которая часто сочетается с паническими атаками, и выраженные побочные эффекты снизили их популярность. Препаратами первой линии выбора стали СИОЗС.[7]
Препаратами первой линии выбора стали СИОЗС.[7]
У пациентов с маниакальными состояниями в анамнезе предпочтительней применение бензодиазепинов, так как, в отличие от антидепрессантов, они не провоцируют манию[8].
Использование так называемых вегетотропных препаратов (анаприлин, пирроксан, беллоид, белласпон) в сочетании с сосудисто-метаболической терапией (циннаризин, кавинтон, трентал, ноотропил, пирацетам, церебролизин) неэффективно, что подрывает веру в возможность излечения и способствует хронизации заболевания.
Не все классы психотропных препаратов одинаково эффективны в отношении паники. При правильном подходе паническое расстройство хорошо поддаётся лечению. Необходим индивидуальный план лечения для каждого больного, который следует разработать пациенту вместе со своим лечащим врачом.
Психотерапия
Психотерапевтическая помощь (помощь психотерапевта или психолога) при паническом расстройстве может помочь осознать психологическую проблему, увидеть способы её решения, проработать психологический конфликт.
Доказана эффективность когнитивно-поведенческой психотерапии при лечении панического расстройства[9][7][8][10] (в том числе когнитивно-поведенческой психотерапии, проводимой через Интернет[11]). По данным мета-анализа, при лечении панических атак когнитивно-поведенческая психотерапия обладала более высоким показателем силы эффекта в сравнении с фармакологическим лечением и комбинированным лечением (то есть психофармакотерапией в сочетании с психотерапией). При использовании когнитивно-поведенческой психотерапии меньшее количество пациентов прерывало лечение по сравнению с фармакологическим и комбинированным лечением[12]. Есть данные о большей противорецидивной активности когнитивно-поведенческой психотерапии при паническом расстройстве в сравнении с фармакотерапией[10]. Когнитивно-поведенческая психотерапия также способствует успешному прекращению приёма бензодиазепинов у пациентов с паническим расстройством и помогает им сохранить терапевтический эффект, не прибегая к лекарствам[13].
В частности, в рамках когнитивно-поведенческой психотерапии для устранения тревожных мыслей, вызывающих паническую атаку, может использоваться метод «остановки мысли»[14]. Может применяться и такая техника, как репликация симптома в лабораторных условиях[15]. Техника репликации симптома в лабораторных условиях заключается в том, что с помощью различных приёмов (гипервентиляция лёгких по Кларку, применение кофеина или быстрый подъём по лестницам) воспроизводятся некоторые из физиологических компонентов панической атаки — потоотделение, учащённое сердцебиение и др. Затем выявляются возникшие у пациента интерпретации этих физических ощущений и эмоциональные реакции. В случае правильной интерпретации пациентом возникших ощущений психотерапевт обращает его внимание на связь между интерпретацией и эмоциональным состоянием («Ты объясняешь сейчас сердцебиение пробегом по лестнице, а не сердечным приступом, и ты абсолютно спокоен»). Терапевт также предлагает пациенту поискать альтернативное объяснение сердцебиению в обыденной жизни вместо уверенности, будто сердцебиение — однозначный признак сердечного приступа, и опираться при этом на лабораторный опыт[15].
В рамках когнитивно-поведенческой психотерапии пациента также могут обучать во время терапевтических сеансов навыкам релаксации, техникам контролируемого дыхания по Кларку, после чего пациенту рекомендуют использовать эти навыки в промежутках между сеансами, во время эпизодов интенсивной тревоги[15].
При лечении панического расстройства применяется также психоанализ. С точки зрения психоаналитиков, основной причиной панического расстройства считаются вытесненные психологические конфликты, которые не находят выхода, не могут быть осознаны и разрешены человеком вследствие различных причин.
Теории о происхождении заболевания
- Серотониновая теория — данные о роли серотонина в патогенезе панических расстройств получены в фармакологических исследованиях. Исследования нейроэндокринных реакций в ответ на введение серотонинергических препаратов выявили у больных паническими расстройствами определённые изменения (изменение секреции кортизола в ответ на введение фенфлурамина и мета-хлорфенилпиперазина).
 Возможно, у больных паническим расстройством изменены содержания связанного с серотонином белка тромбоцитов. Также проводились исследования о связи панического расстройства с выработкой антител к серотонину. Имеет значение взаимодействие серотонинергической и других нейромедиаторных систем. Связь между серотонинергической и норадреналинергической системами позволяют объяснить нарушение вегетативной регуляции при паническом расстройстве. СИОЗС могут также уменьшать симптомы панического расстройства опосредованно, через влияние на норадренергическую систему. Например, флуоксетин способен нормализовать MHPG-реакцию на введение клонидина у больных с паническим расстройством.
Возможно, у больных паническим расстройством изменены содержания связанного с серотонином белка тромбоцитов. Также проводились исследования о связи панического расстройства с выработкой антител к серотонину. Имеет значение взаимодействие серотонинергической и других нейромедиаторных систем. Связь между серотонинергической и норадреналинергической системами позволяют объяснить нарушение вегетативной регуляции при паническом расстройстве. СИОЗС могут также уменьшать симптомы панического расстройства опосредованно, через влияние на норадренергическую систему. Например, флуоксетин способен нормализовать MHPG-реакцию на введение клонидина у больных с паническим расстройством. - Респираторные теории — объясняют возникновение панического расстройства сбоем в регуляции дыхания и возникновением «аварийной» реакции. Паническая атака провоцируется чрезмерностью дыхания через активизацию предполагаемого «центра удушья».
- Нейроанатомическая модель предполагает, что паническая атака связана с гиперактивацией стволовых структур, что проявляется в изменении дыхательных функций, дисфункции серотонинергических и норадреналинергических структур.
 Остальные проявления данная модель связывает с нарушениями функционирования других отделов мозга — лимбические структуры — тревога ожидания, нарушения в префронтальной коре — ограничительное поведение.
Остальные проявления данная модель связывает с нарушениями функционирования других отделов мозга — лимбические структуры — тревога ожидания, нарушения в префронтальной коре — ограничительное поведение.
- Нейроанатомическая модель предполагает, что паническая атака связана с гиперактивацией стволовых структур, что проявляется в изменении дыхательных функций, дисфункции серотонинергических и норадреналинергических структур.
- Генетические гипотезы — попытка определения генетических локусов, ответственных за развитие панического расстройства, остаётся без успеха до сих пор. Паническое расстройство часто встречается у близких родственников, что может говорить о роли наследственности. Также была установлена коморбидность с такими заболеваниями, как биполярное аффективное расстройство, алкоголизм.
- Вегетативные теории основаны на изучении кардиальных показателей взаимодействия парасимпатической и симпатической систем и реакций на норадренергические препараты (исследования с клонидином). У взрослых больных обнаружено сглаживание кривой секреции гормона роста в ответ на введение клонидина, что указывает на снижение чувствительности гипоталамических α2-адренорецепторов, также наблюдается повышение артериального давления и уровня MHPG.
 При успешном лечении панического расстройства происходит восстановление нормальной реакции в виде снижения MHPG в ответ на введение клонидина.
При успешном лечении панического расстройства происходит восстановление нормальной реакции в виде снижения MHPG в ответ на введение клонидина.- Locus ceruleus модель — при введении йохимбина и агонистов α2-адренорецепторов стимулирующих locus ceruleus наблюдается увеличение тревоги.
- Условно-рефлекторная теория — предположительно, любая тревожная реакция возникает в результате взаимодействия миндалины со стволовыми структурами, базальными ганглиями, гипоталамусом и корковыми путями. Внутренние стимулы рассматриваются как условные стимулы, способные запускать паническую атаку. Паническая атака возникает в результате активации нервных путей, обеспечивающих возникновение условно-рефлекторной фобической реакции в ответ на нормальные колебания физиологических функций. Подтверждает эту теорию и то, что на основе дыхательной и физиологической реакции на вдыхание углекислого газа можно выработать условный рефлекс.
- Когнитивные теории — предположительно, на развитие панических атак влияет ряд когнитивных факторов. У больных с паническим расстройством наблюдается повышенная тревожная чувствительность и снижение порога восприятия сигналов от внутренних органов. Такие люди сообщают о более значительном числе симптомов при провокации тревоги физической нагрузкой.
См. также
Примечания
- ↑ Всемирная организация здравоохранения. F4 Невротические, связанные со стрессом, и соматоформные расстройства // Международная классификация болезней (10-й пересмотр). Класс V: Психические расстройства и расстройства поведения (F00—F99) (адаптированный для использования в Российской Федерации). — Ростов-на-Дону: Феникс, 1999. — С. 175—176. — ISBN 5-86727-005-8.
- ↑ 1 2 3 Голощапов А., 2016, Глава 6. Паническое расстройство (панические атаки) 6.1. Что такое паническое расстройство?.
- ↑ Голощапов А., 2016, 6.2. Специфические стратегии работы с паническим расстройством 6.1. Способы пережить паническую атаку.
- ↑ Shear M. K., Brown T. A., Barlow D. H., Money R., Sholomskas D. E., Woods S. W., Gorman J. M., Papp L. A. Multicenter collaborative panic disorder severity scale. (англ.) // The American Journal Of Psychiatry. — 1997. — November (vol. 154, no. 11). — P. 1571—1575. — doi:10.1176/ajp.154.11.1571. — PMID 9356566. []
- ↑ http://goodmedicine.org.uk/files/panic,%20assessment%20pdss.pdf
- ↑ APA Diagnostic Classification DSM-IV-TR
- ↑ 1 2 3 Каспер З., Зоар Дж., Стейн Д. Принятие решений в психофармакотерапии / Пер. с англ. В. Штенгелов. — Киев: Сфера, 2006. — 136 с. — ISBN 966-8782-24-0.
- ↑ 1 2 3 Фармакотерапия в неврологии и психиатрии: [Пер. с англ.] / Под ред. С. Д. Энна и Дж. Т. Койла. — Москва: ООО: «Медицинское информационное агентство», 2007. — 800 с.: ил. с. — 4000 экз. — ISBN 5-89481-501-0.
- ↑ Kaczkurkin A. N., Foa E. B. Cognitive-behavioral therapy for anxiety disorders: an update on the empirical evidence. (англ.) // Dialogues In Clinical Neuroscience. — 2015. — September (vol. 17, no. 3). — P. 337—346. — PMID 26487814. []
- ↑ 1 2 Городничев А.В. Современные тенденции в терапии тревожных расстройств: от научных данных к клиническим рекомендациям // Биологические методы терапии психических расстройств (доказательная медицина — клинической практике) / Под ред. С.Н. Мосолова. — Москва : Издательство «Социально-политическая мысль», 2012. — С. 643—668. — 1080 с. — 1000 экз. — ISBN 978-5-91579-075-8.
- ↑ Hedman E., Ljótsson B., Rück C., Bergström J., Andersson G., Kaldo V., Jansson L., Andersson E., Andersson E., Blom K., El Alaoui S., Falk L., Ivarsson J., Nasri B., Rydh S., Lindefors N. Effectiveness of internet-based cognitive behaviour therapy for panic disorder in routine psychiatric care. (англ.) // Acta Psychiatrica Scandinavica. — 2013. — December (vol. 128, no. 6). — P. 457—467. — doi:10.1111/acps.12079. — PMID 23406572. []
- ↑ Холмогорова А. Б., Гаранян Н. Г., Никитина И. В., Пуговкина О. Д. Научные исследования процесса психотерапии и ее эффективности: современное состояние проблемы. Часть 1 // Социальная и клиническая психиатрия. — 2009. — Т. XIX, № 3. — С. 92—100.
- ↑ Otto M. W., Hong J. J., Safren S. A. Benzodiazepine discontinuation difficulties in panic disorder: conceptual model and outcome for cognitive-behavior therapy. (англ.) // Current Pharmaceutical Design. — 2002. — Vol. 8, no. 1. — P. 75—80. — doi:10.2174/1381612023396726. — PMID 11812251. []
- ↑ Martha Davis, Elizabeth Robbins Eshelman, Matthew McKay. The relaxation & stress reduction workbook. — Oakland, USA: New Harbiner Publications Inc., 2008. — 294 с. — ISBN 1-57224-214-0.
- ↑ 1 2 3 Гаранян Н. Г. Практические аспекты когнитивной психотерапии // Московский психотерапевтический журнал. — 1996. — № 3.
Литература
- Клиническое руководство по психическим расстройствам / Под ред. Д. Барлоу. Перевод с английского под ред. профессора Э.Г. Эйдемиллера. — 3-е изд. — Санкт-Петербург: Питер, 2008. — 912 с. — ISBN 978-5-94723-046-8.
- Варфоломеева Ю. Е. Коморбидность панического расстройства // Независимый психиатрический журнал. — 2014. — № 1.
- Голощапов А. Тревога, страх и панические атаки. Книга самопомощи (рус.). — ИГ «Весь», 2016. — ISBN 978-5-9573-3069-1.
Ссылки
Симпато-адреналовые кризы, причины и лечение | Сидя дома
Симпато-адреналовый криз чаще всего является одним из проявлений соматоформной дисфункции(ВСД) по гипертензивному типу. В вегетативной нервной системе человека существует два отдела, симпатический и парасимпатический. Симпатический отвечает за возбуждение организма. Он преобладает над парасимпатическим при физических нагрузках, пробуждении после сна, психоэмоциональных стрессах. Существенное преобладание симпатического отдела вызывает симпато-адреналовые кризы. Происходит это следующим образом. Человек испытывает страх к чему-либо, тревога нарастает, может перерасти в панику, тем временем мозг посылает сигналы о реальной опасности к надпочечникам, чтобы выбросить большую дозу адреналина.
Специфического лечения они, как правило, не требуют. Но все же следует пресекать то, от чего они чаще всего возникают. Основными причинами чаще всего являются несбалансированное питание, неправильный образ жизни и стрессы. Также следует обратить внимание на гормоны щитовидной железы и обследовать сердечно-сосудистую систему. Если по результатам обследования там все будет в норме, то причина кроется вероятнее всего в образе жизни и стрессах.
Но если все-таки криз случился, то лучше его быстрее купировать, иначе в организме будет ощущение усталости и разбитости. Криз обычно начинается «по-нарастающей», а уже после достигает своего пика. По продолжительности чаще всего бывает от часа до трех.
Как только вы поняли, что криз начинается, сразу осознайте, что ничего опасного в этом нет. Успокойтесь и (очень важно) расслабьтесь, расслабьте мышцы, иначе давление будет расти и дальше. Медикаментозная терапия чаще всего не требуется, а при мысли померить давление, человек обычно сам себе его еще выше поднимает, потому что начинает нервничать еще больше от страха, что оно высокое.
Но если все же вы решили его измерить и оно повышено, то можете принять Каптоприл в рекомендуемой врачом дозе, а при выраженной тахикардии Анаприлин. Опять же, дозы регулируются врачом.
Чтобы добиться отсутствия кризов советуем вам постараться вести правильный образ жизни, больше находиться на свежем воздухе, проявлять физическую активность и сбалансированно питаться.
Желаем вам не болеть!
Вегето-сосудистые кризы («Панические атаки») | Статьи клиники Медсервис
Вегето-сосудистый криз – внезапный сбой в работе вегетативной нервной системы. «Паническое» расстройство обычно начинается в молодом возрасте, реже — в детском и зрелом. Женщины болеют чаще в 2-3 раза.
Факторы, вызывающие вегето-сосудистые кризы: острые и хронические психоэмоциональные и социально – бытовые стрессовые ситуации, воздействие физических и психических факторов, инфекции (вирусные), хронический алкоголизм и табачная интоксикация, гиподинамия, дисгормональные расстройства, умственное и физическое переутомление.
Основной клинической особенностью пациентов с вегето-сосудистыми кризами является наличие у них многочисленных жалоб.
При симпатоадреналовом кризе появляется или усиливается головная боль, возникает онемение и похолодание конечностей, бледность лица, повышается артериальное давление, учащается пульс, отмечаются боли в области сердца, появляется чувство тревоги и страха смерти, ознобоподобный тремор, иногда повышается температура до 38 -39 градусов.
Вагоинсулярный криз проявляется ощущением жара в голове и лице, удушья, могут возникнуть тошнота, слабость, потливость, головокружение, позывы на дефекацию, отмечается урежение пульса и снижение артериального давления.
Смешанные кризы характеризуются сочетанием симптомов либо поочередным их проявлением.
Диагноз вегето-сосудистых кризов ставится путём исключения других заболеваний, способных вызвать подобные состояния – это и ишемическая болезнь сердца, гипертоническая болезнь, сахарный диабет, заболевания щитовидной железы, почек, надпочечников, заболевания нервной системы. Проводятся различные обследования — МРТ, СКТ, ЭХОКГ, холтер, СМАД, УЗИ внутренних органов, различные анализы. Все эти обследования можно сделать в нашей клинике «Медсервис» и получить квалифицированную консультацию любого специалиста.
Симпатоадреналовый криз и панические атаки
Симпато-адреналовый криз (развивается как следствие превалирования одного из отделов нервной системы над другим, а именно симпатического над парасимпатическим).
Патология характеризуется проявлениями панической тревоги, ознобом, нехваткой воздуха, онемением конечностей, губ и языка, тахикардией (учащённым сердцебиением), ощущением боли в сердце, шумом в ушах, нарушением зрения.
Проводя осмотр, врач отмечает: пилоэрекцию (появление «гусиной кожи»), дрожание (тремор) губ, рук и век, небольшой подъём температуры тела, а также некоторое повышение артериального давления.
Приступ может прекращаться неожиданно, сопровождаясь обильным мочеиспусканием (моча светлая и имеет низкую относительную плотность). Часто, период выхода может затягиваться на несколько часов или даже суток, сопровождаясь выраженными явлениями астении.
Симпато-адреналовый криз – одно из проявлений панического расстройства. Повторяющиеся панические атаки существенно осложняют жизнь человеку, испытывающему подобные состояния. И, хотя они не являются прямой угрозой жизни, последствия для социальной и психологической сфер жизни пациента могут быть очень значительными.
Подразделение панических приступов по степени тяжести- Лёгкая степень – приступы длятся не более 15 минут, выражены небольшим количеством симптомов, имеют вегетативные сдвиги в пределах нормальных колебаний.
- Средняя степень тяжести – продолжительность от 15 минут до часа, выраженные сдвиги вегетативного характера, наличие различных симптомов: ощущение тревоги, страха. После приступа наблюдается выраженная астения (сильная слабость, отсутствие концентрации, мышечные боли, раздражительность, головная боль, диспепсия, головокружение). Она может длиться до полутора суток.
- Тяжёлая степень – длятся более часа, сопровождаются значительно выраженными вегетативными расстройствами, большим количеством симптомов, в том числе тонические судороги, ознобоподобный гиперкинез (чувство внутренней дрожи, неожиданно возникающий озноб, сопровождающийся появлением так называемой «гусиной кожи» и внутренним напряжением), чувство страха. Быстро развивается астения и продолжаться она может до 3 – 4 суток.
Сопровождающие симпато-адреналовый криз симптомы имеют прямое отношение к происходящему при нём выбросу слишком большого количества адреналина.
- Паническая тревога, жалобы на страх смерти, необъяснимая тоска.
- В отношении сердца: замирание и перебои, боли, учащённое сердцебиение.
- Чувство нехватки воздуха.
- Пульсирующая головная боль.
- Озноб, дрожь.
- Нарушение зрения.
- Шум в ушах.
- Онемение губ, языка, конечностей.
- Галлюцинации, дезориентация.
Панические атаки, могут быть единственным проявлением тревожного расстройства или сочетаться с постоянной тревогой, беспокойством, повышенной утомляемостью, плохой переносимости физической нагрузки, ипохондрией и депрессией.
Считают, что непосредственной причиной панической атаки является выброс центральными адренергическими системами и надпочечниками в кровь повышенного содержания адреналина, серотонина и других нейротрансмиттеров.
Важную роль в происхождении панических атак играет наследственная предрасположенность, которая определяется снижением порога возбуждения норадренергических и серотонинергических ядер ствола мозга, нарушением нейромедиаторных процессов в лимбической системе.
Лечение панических атак включает применение альфа-адреноблокатора Пророксан который блокирует передачу нервного возбуждения в области адренорецепторов за счет нарушения взаимодействия медиатора с адренореактивными системами, не влияя на передачу возбуждения в ганглиях и не изменяя процессы образования медиатора и выделения его из постганглионарных нервных окончаний
Пророксан смягчает адренореактивность у больных с нейроциркуляторной дистонией по гипертоническому типу, а также положительно влияет на ауторегуляцию мозгового кровотока — ослабление проявлений вегетативных пароксизмов. (М. В. Васин 2002).
В случаях, когда вегетативный криз сопровождается психическими нарушениями, протекающими с симпато-адреналовым синдромом, Пророксан является препаратом выбора.
Острый кризис надпочечников — (Аддисонский кризис)
Связанный : Условия надпочечников | Адренокортикальная карцинома | Кризис надпочечников | Компьютерная томография | Кушинга | Эндоскопический | Гиперальдостеронизм | Недостаточность | Лапароскопический | Феохромоцитома | Галерея шрамов | Что такое надпочечники?
Что такое острый кризис надпочечников (аддисонский кризис)?
Определение:
Острый надпочечниковый криз — это опасное для жизни состояние, вызванное недостаточным уровнем кортизола, гормона, вырабатываемого и выделяемого надпочечниками.
Альтернативные названия: Кризис надпочечников; Аддисонский кризис; Острая надпочечниковая недостаточность
Причины, частота возникновения и факторы риска:
Два надпочечника расположены над почками. Они состоят из внешней части, называемой корой, и внутренней части, называемой мозговым веществом. Кора головного мозга производит три типа гормонов, все из которых называются кортикостероидами.
Кортизол — это глюкокортоид, кортикостероид, который поддерживает регуляцию уровня глюкозы (сахара в крови), подавляет иммунный ответ и высвобождается как часть реакции организма на стресс.Производство кортизола регулируется небольшой железой чуть ниже мозга, называемой гипофизом. Кортизол необходим для жизни. Острый надпочечниковый криз — это неотложная медицинская помощь, вызванная недостатком кортизола. Пациенты могут испытывать дурноту или головокружение, слабость, потоотделение, боль в животе, тошноту и рвоту или даже потерю сознания.
Кризис надпочечников возникает при ухудшении состояния надпочечников (болезнь Аддисона, первичная надпочечниковая недостаточность), при повреждении гипофиза (вторичная надпочечниковая недостаточность) или при недостаточном лечении надпочечников.Факторы риска надпочечникового криза включают физический стресс, такой как инфекция, обезвоживание, травма или операция, повреждение надпочечников или гипофиза, а также преждевременное прекращение лечения стероидами, такими как преднизон или гидрокортизон.
Симптомы:
- Головная боль
- Глубокая слабость
- Усталость
- Медленные, вялые движения
- Тошнота
- Рвота
- Низкое кровяное давление
- Обезвоживание
- Высокая температура
- Дрожащая дрожь или озноб a
- Потемнение кожи
- Учащенное сердцебиение
- Боль в суставах
- Боль в животе
- Непреднамеренная потеря веса
- Ускоренное дыхание (см. Тахипноэ)
- Необычное и чрезмерное потоотделение на лице и / или ладонях
- Кожная сыпь или могут присутствовать поражения
- Боль в боку
- Потеря аппетита
Признаки и тесты:
- Тест на стимуляцию АКТГ (коррозин) показывает низкий уровень кортизола.
- Базовый уровень кортизола низкий.
- Уровень сахара в крови натощак может быть низким.
- Калий в сыворотке повышен (обычно первичная надпочечниковая недостаточность).
- Уровень натрия в сыворотке снижен (обычно первичная надпочечниковая недостаточность).
Лечение:
При кризе надпочечников необходимо немедленно сделать внутривенную или внутримышечную инъекцию гидрокортизона (инъекционный кортикостероид). Обычно необходимо поддерживающее лечение низкого кровяного давления с помощью внутривенных вливаний.Госпитализация необходима для адекватного лечения и наблюдения. Если причиной криза стала инфекция, может потребоваться антибактериальная терапия.
Ожидания (прогноз):
Смерть может наступить из-за сильнейшего шока, если не будет обеспечено раннее лечение.
Осложнения:
Звонок своему врачу:
Позвоните своему врачу, если у вас болезнь Аддисона и вы не можете принимать обычные лекарства из-за рвоты.Обратитесь в отделение неотложной помощи или позвоните на местный номер службы экстренной помощи (например, 911), если развиваются симптомы острого криза надпочечников.
Профилактика:
Людей, страдающих болезнью Аддисона, необходимо научить распознавать признаки потенциального стресса, который может вызвать острый надпочечниковый кризис. Большинство людей с болезнью Аддисона учат делать себе экстренную инъекцию гидрокортизона или увеличивать дозу перорального преднизона во время стресса.
Для человека, страдающего болезнью Аддисона, важно всегда иметь при себе медицинскую карточку, в которой указан тип лекарства и правильная доза, необходимая в случае возникновения чрезвычайной ситуации.
Никогда не пропускайте лекарства. Если вы не можете удержать лекарство из-за рвоты, сообщите об этом врачу.
Рекомендации по лечению надпочечников: Краткое изложение рекомендаций
Автор
Лиза Киркланд, доктор медицины, FACP, FCCM, MSHA Доцент кафедры внутренней медицины, отделение госпитальной медицины, клиника Мэйо; Заведующий отделением интенсивной терапии, терапевты ANW, Abbott Northwestern Hospital
Лиза Киркланд, доктор медицины, FACP, FCCM, MSHA является членом следующих медицинских обществ: Американского колледжа врачей, Общества реаниматологии, Общества госпитальной медицины
Раскрытие: Ничего не раскрывать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие: Получил зарплату от Medscape за работу. для: Medscape.
Главный редактор
Джордж Т. Гриффинг, доктор медицины Почетный профессор медицины, медицинский факультет Университета Сент-Луиса
Джордж Т. Гриффинг, доктор медицины, является членом следующих медицинских обществ: Американской ассоциации содействия развитию науки, Международного общества клинической денситометрии, Южного Общество клинических исследований, Американский колледж руководителей медицинской практики, Американская ассоциация руководителей врачей, Американский колледж врачей, Американская диабетическая ассоциация, Американская федерация медицинских исследований, Американская кардиологическая ассоциация, Центральное общество клинических и трансляционных исследований, Эндокринное общество
Раскрытие информации : Нечего раскрывать.
Дополнительные участники
Дэвид М. Клачко, доктор медицинских наук Почетный профессор кафедры внутренней медицины, отделение эндокринологии, диабета и метаболизма, Медицинская школа Университета Миссури-Колумбия
Дэвид Клачко, доктор медицинских наук, доктор медицинских наук является членом следующих организаций медицинские общества: Alpha Omega Alpha, Медицинская ассоциация штата Миссури, Американский колледж врачей — Американское общество внутренней медицины, Американская диабетическая ассоциация, Американская федерация медицинских исследований, Эндокринное общество, Sigma Xi
Раскрытие: нечего раскрывать.
Лечение и лечение надпочечникового кризиса: медицинское обслуживание, консультации
Автор
Лиза Киркланд, доктор медицины, FACP, FCCM, MSHA Доцент кафедры внутренней медицины, отделение госпитальной медицины, клиника Мэйо; Заведующий отделением интенсивной терапии, терапевты ANW, Abbott Northwestern Hospital
Лиза Киркланд, доктор медицины, FACP, FCCM, MSHA является членом следующих медицинских обществ: Американского колледжа врачей, Общества реаниматологии, Общества госпитальной медицины
Раскрытие: Ничего не раскрывать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие: Получил зарплату от Medscape за работу. для: Medscape.
Главный редактор
Джордж Т. Гриффинг, доктор медицины Почетный профессор медицины, медицинский факультет Университета Сент-Луиса
Джордж Т. Гриффинг, доктор медицины, является членом следующих медицинских обществ: Американской ассоциации содействия развитию науки, Международного общества клинической денситометрии, Южного Общество клинических исследований, Американский колледж руководителей медицинской практики, Американская ассоциация руководителей врачей, Американский колледж врачей, Американская диабетическая ассоциация, Американская федерация медицинских исследований, Американская кардиологическая ассоциация, Центральное общество клинических и трансляционных исследований, Эндокринное общество
Раскрытие информации : Нечего раскрывать.
Дополнительные участники
Дэвид М. Клачко, доктор медицинских наук Почетный профессор кафедры внутренней медицины, отделение эндокринологии, диабета и метаболизма, Медицинская школа Университета Миссури-Колумбия
Дэвид Клачко, доктор медицинских наук, доктор медицинских наук является членом следующих организаций медицинские общества: Alpha Omega Alpha, Медицинская ассоциация штата Миссури, Американский колледж врачей — Американское общество внутренней медицины, Американская диабетическая ассоциация, Американская федерация медицинских исследований, Эндокринное общество, Sigma Xi
Раскрытие: нечего раскрывать.
Механизмы вегетативной недостаточности, связанной с гипогликемией, и ее составляющие синдромы при диабете
Реферат
Ятрогенная гипогликемия — это проблема для людей с диабетом. Это вызывает повторяющиеся заболевания, а иногда и смерть, а также порочный цикл повторяющейся гипогликемии, препятствуя поддержанию эугликемии на протяжении всей жизни диабета. Улучшенные терапевтические подходы, которые сведут к минимуму как гипо-, так и гипергликемию, будут основаны на понимании патофизиологии глюкорегуляции, в частности, контррегуляции глюкозы, при инсулино-дефицитном (тип 1 и продвинутый тип 2) диабет.У таких пациентов гипогликемия является результатом взаимодействия относительного или абсолютного терапевтического избытка инсулина и нарушенной физиологической (синдром дефектной контррегуляции глюкозы) и поведенческой (синдром неосведомленности о гипогликемии) защиты от падения концентрации глюкозы в плазме. Концепция вегетативной недостаточности, связанной с гипогликемией (HAAF) при диабете, предполагает, что недавняя предшествующая ятрогенная гипогликемия вызывает как нарушение контррегуляции глюкозы (за счет снижения реакции адреналина на заданный уровень последующей гипогликемии в условиях отсутствия снижения инсулина и отсутствия прироста глюкагона). и неосведомленность о гипогликемии (за счет снижения симпатоадреналовой функции и возникающих в результате нейрогенных симптомов реакции на заданный уровень последующей гипогликемии) и, таким образом, порочный круг повторяющейся гипогликемии.Клиническое влияние HAAF хорошо известно при диабете 1 типа; он также влияет на людей с прогрессирующим диабетом 2 типа. В настоящее время известно, что это в значительной степени обратимо — всего за 2–3 недели тщательного предотвращения гипогликемии у большинства больных. Однако механизмы HAAF и составляющих его синдромов в значительной степени неизвестны. Потеря секреторной реакции глюкагона, ключевой признак дефектной контррегуляции глюкозы, правдоподобно объясняется дефицитом инсулина, в частности, потерей декремента инсулина внутри островка, который обычно сигнализирует о секреции глюкагона при падении уровня глюкозы.Уменьшение нейрогенных симптомов — ключевой признак незнания гипогликемии — в значительной степени является результатом снижения симпатических нервных реакций на падение уровня глюкозы. Механизм, с помощью которого гипогликемия смещает гликемический порог активации симпатоадреналовой функции в сторону более низких концентраций глюкозы в плазме, ключевой особенности обоих компонентов HAAF, неизвестен. Это, по-видимому, не является результатом высвобождения системного медиатора (например, кортизола, адреналина) во время предшествующей гипогликемии или повышенного транспорта глюкозы из крови в мозг (хотя возможно увеличение транспорта альтернативных видов топлива).Вероятно, это результат изменения метаболизма мозга. Хотя существует множество подсказок, конкретное изменение еще предстоит определить. Хотя основное внимание в исследованиях уделялось гипоталамусу, теперь известно, что гипогликемия активирует обширные области мозга, включая медиальную префронтальную кору. Также была высказана возможность того, что HAAF может быть результатом постгипогликемической суперкомпенсации гликогена в головном мозге. Наконец, по-видимому, существуют различные причины HAAF. Помимо недавней предшествующей гипогликемии, к ним относятся HAAF, связанные с физическими упражнениями и сном.Ясно, что объединяющий механизм HAAF также должен учитывать эти причины. В ожидании профилактики и лечения диабета необходимы важные фундаментальные, трансляционные исследования и исследования результатов, если мы хотим исключить гипогликемию из жизни людей, страдающих диабетом.
КЛИНИЧЕСКАЯ ПРОБЛЕМА
Ятрогенная гипогликемия является лимитирующим фактором в гликемическом управлении диабетом (1). Он вызывает рецидивирующие заболевания у большинства людей с диабетом 1 типа и многих людей с диабетом 2 типа, а иногда и со смертельным исходом.Кроме того, эпизоды гипогликемии, даже бессимптомные эпизоды, ослабляют защиту от последующей гипогликемии, вызывая вегетативную недостаточность, связанную с гипогликемией (HAAF), клинические синдромы недостаточной контррегуляции глюкозы и неосведомленности о гипогликемии, и, следовательно, порочный цикл повторяющейся гипогликемии. Кроме того, барьер гипогликемии препятствует поддержанию эугликемии на протяжении всей жизни диабета и, таким образом, полной реализации преимуществ контроля гликемии. Гликемические цели, пропагандируемые профессиональными диабетическими организациями, негласно признают этот барьер.Никто не рекомендует использовать нормальный HbA 1c . Хотя гликемический контроль за исключением эугликемии снижает (но не устраняет) микрососудистые осложнения диабета, долгосрочная эугликемия может быть необходима для уменьшения макрососудистых осложнений у значительной части людей с диабетом (1).
Несмотря на неуклонное улучшение гликемического контроля при диабете (2) и, возможно, из-за стимула к гликемическому контролю, который стал результатом положительных результатов исследования по контролю диабета и осложнений (3) и U.K. Проспективное исследование диабета (4,5), популяционные данные показывают, что гипогликемия продолжает оставаться проблемой для людей с диабетом 1 (6) и 2 (7,8) типа. Проблема не ограничивается диабетом 1 типа (1). При диабете 2 типа, принимаемом инсулином, частота случаев тяжелой гипогликемии, по крайней мере, требующей неотложного лечения, приближается к таковой при диабете 1 типа (7,8).
Устранение гипогликемии из жизни людей с диабетом и долгосрочное поддержание эугликемии, несомненно, потребуют замены или секреции инсулина, регулируемого глюкозой.В ожидании достижения этой конечной цели существует острая необходимость в разработке терапевтических подходов, которые минимизируют как гипер-, так и гипогликемию. Предполагается, что эти улучшенные подходы будут основаны на понимании патофизиологии глюкорегуляции, в частности, противорегуляции глюкозы при диабете 1 и 2 типа. Эта комплексная патофизиология была рассмотрена (1). Здесь основное внимание уделяется тому, что известно, а что неизвестно, о механизмах клинических синдромов дефектной контррегуляции глюкозы и гипогликемии, а также концепции HAAF при инсулино-дефицитном (тип 1 и продвинутый тип 2) диабете. .
ПАТОФИЗИОЛОГИЯ ПРОТИВОРЕГУЛЯЦИИ ГЛЮКОЗЫ ПРИ ДИАБЕТЕ
Ключевыми компонентами физиологии контррегуляции глюкозы, механизмами, которые обычно предотвращают или быстро корректируют гипогликемию, являются 1 ) снижение секреции инсулина β-клетками поджелудочной железы 2 ) увеличение секреции глюкагона α-клетками панкреатических островков и, в отсутствие последнего, 3 ) увеличение адреномедуллярной секреции адреналина (9). Все три защиты от развития гипогликемии нарушены при инсулино-дефицитном диабете (тип 1 и прогрессирующий тип 2) (1).У таких пациентов ятрогенная гипогликемия является результатом взаимодействия относительного или абсолютного избытка инсулина, который должен время от времени происходить из-за фармакокинетических недостатков всех терапевтических схем инсулина, а также из-за нарушенной контррегуляции глюкозы. При падении концентрации глюкозы в плазме 1 ) концентрации инсулина в плазме не снижаются (при отсутствии эндогенной секреции инсулина это просто результат абсорбции и клиренса введенного инсулина), 2 ) концентрации глюкагона в плазме не повышаются ( вероятно, это результат отсутствия сигнала внутри островка инсулина, снижение уровня инсулина внутри островка и, таким образом, тоническое ингибирование α-клеток инсулином [10–13], как обсуждается ниже), и 3 ) концентрации адреналина в плазме повышаются, но инкремент обычно снижается (гликемический порог активации симпатоадреналовой функции обычно смещен в сторону более низких концентраций глюкозы в плазме).Последнее, критическая особенность патофизиологии противорегуляции глюкозы, обычно является результатом недавней предшествующей ятрогенной гипогликемии, хотя сон и, в некоторой степени, предшествующие упражнения имеют аналогичный эффект (1).
Ослабленный адреномедуллярный адреналиновый ответ на падение концентрации глюкозы в плазме в условиях отсутствия ответов β-клеточного инсулина и α-клеточного глюкагона вызывает клинический синдром дефектной контррегуляции глюкозы (1). Риск тяжелой ятрогенной гипогликемии повышается в 25 или более раз при агрессивной гликемической терапии (14,15).Ослабленный симпатоадреналовый ответ (в основном ослабленный симпатический нервный [16] ответ, как обсуждается ниже) вызывает клинический синдром неосведомленности о гипогликемии (1). У таких пациентов риск тяжелой ятрогенной гипогликемии увеличивается примерно в шесть раз во время агрессивной гликемической терапии (17).
HAAF ПРИ ДИАБЕТЕ
Концепция HAAF при диабете типа 1 (18) и распространенного типа 2 (19) предполагает, что недавняя предшествующая ятрогенная гипогликемия вызывает как нарушение контррегуляции глюкозы (за счет снижения реакции адреналина до заданного уровня последующей гипогликемии в установка отсутствующего снижения инсулина и отсутствующего прироста глюкагона) и неосведомленность о гипогликемии (за счет снижения симпатоадреналовых и возникающих в результате нейрогенных симптомов реакции на заданный уровень последующей гипогликемии) и, таким образом, порочный цикл повторяющейся гипогликемии (1) (рис.1). Концепция HAAF была расширена за счет включения HAAF, связанного со сном и физическими упражнениями (1) (рис. 1). Поскольку как нарушение регуляции глюкозы (14,15), так и неосведомленность о гипогликемии (17) приводят к значительному увеличению частоты тяжелой гипогликемии, вегетативной, особенно симпатоадреналовой, недостаточность, вызванная недавней предшествующей гипогликемией, или физическими упражнениями или сном, связана с высокой частотой клинической гипогликемии у людей с инсулино-дефицитным (тип 1 и запущенный тип 2) диабетом (1).
Снижение симпатоадреналовой активности играет ключевую роль в патогенезе как дефектной контррегуляции глюкозы (снижение адреномедуллярного действия адреналина), так и неосведомленности о гипогликемии (в значительной степени сниженное симпатическое нервное [адренергическое и холинергическое] действие) и, следовательно, HAAF при диабете (1). Эти пониженные действия в значительной степени, возможно исключительно, являются результатом снижения активации симпатоадреналовой функции и, как следствие, снижения высвобождения его биологически активных продуктов (например, адреналина, норэпинефрина, ацетилхолина) в ответ на заданный уровень гипогликемии (т.е. сдвиг гликемических порогов в сторону более низких концентраций глюкозы в плазме), а не снижение чувствительности тканей к действию этих гормонов / нейротрансмиттеров. Имеются убедительные доказательства того, что метаболическая (и гемодинамическая) чувствительность всего тела к адреналину не снижается у пациентов с диабетом 1 типа (20,21). Аналогичным образом, местная метаболическая чувствительность жировой ткани и скелетных мышц к β 2 -адренергическому агонисту (тербуталин), по-видимому, не снижается (22). С другой стороны, есть некоторые доказательства того, что снижение β-адренергической чувствительности может вносить вклад в патогенез незнания гипогликемии (23–26).Эти доказательства включают снижение хронотропной чувствительности сердца к неселективному β-адренергическому агонисту изопротеренолу у пациентов с сахарным диабетом 1 типа и неосведомленностью о гипогликемии (23, 24), а также устранение сниженной β-адренергической чувствительности и неосведомленности после периода скрупулезного избегания ятрогенной гипогликемии ( 25). Fritsche et al. (26) оценили влияние недавней предшествующей гипогликемии на хронотропную чувствительность сердца к изопротеренолу. Их данные показали, что за гипогликемией следует повышение сердечной β-адренергической чувствительности у недиабетиков, но снижение сердечной β-адренергической чувствительности у пациентов с диабетом 1 типа.де Галан и др. (27) не обнаружили различий в сосудорасширяющей (усиление кровотока в предплечье) ответе на инфузию в плечевую артерию β 2 -адренергического агониста (сальбутамола) у пациентов с неосведомленностью о гипогликемии по сравнению с контрольными субъектами с осознанным и недиабетическим статусом. Если пониженная чувствительность играет роль в патогенезе незнания гипогликемии, необходимо постулировать, что в дополнение к снижению β-адренергической чувствительности пониженная холинергическая чувствительность объясняет уменьшение холинергических симптомов, таких как потоотделение.
Интегрированная (всего тела) гликемическая чувствительность к адреналину (увеличение скорости появления глюкозы [выработка эндогенной глюкозы] и концентрации глюкозы в плазме, продуцируемой гормоном) увеличивается при диабете 1 типа (20). В исследовании пациентов с диабетом 1 типа и недиабетиков Афтаб Гай и соавт. (28) измеряли реакцию на инфузию адреналина в дозе, которая увеличивала концентрацию адреналина в плазме в 25 раз во время 2-часового гиперинсулинемико-эугликемического зажима. В течение последних 30 минут зажимов у пациентов с диабетом 1 типа наблюдалось меньшее увеличение скорости появления глюкозы по сравнению с инсулино-подавленной скоростью в отсутствие инфузии адреналина и меньшее снижение скорости исчезновения глюкозы по сравнению с (частично) инсулино-стимулированной скоростью. при отсутствии инфузии адреналина.Однако более низкие показатели появления глюкозы были связаны с более низкими концентрациями глюкагона в плазме у пациентов, а обнаружение исчезновения глюкозы было результатом более низких показателей индуцированного инсулином исчезновения глюкозы (то есть инсулинорезистентности) в отсутствие инфузии адреналина у пациентов. Вывод о том, что пациенты с диабетом 1 типа демонстрируют пониженную гликемическую реакцию на адреналин при явно гиперинсулинемических состояниях, противоречит доказательствам того, что гликемическая чувствительность к адреналину, по результатам исследования зависимости концентрации адреналина в плазме от уровня глюкозы и концентрации глюкозы в плазме у пациентов с диабетом 1 типа и контрольной группы у пациентов с фиксированными базальными концентрациями инсулина и глюкагона и без них (20) повышается, а не снижается при диабете 1 типа.Берк и др. (20) подтвердили, что гликемическая чувствительность к адреналину повышена у пациентов с диабетом 1 типа, но обнаружили, что она сопоставима у пациентов с диабетом 1 типа и недиабетиков, когда последние, как и пациенты, не могли увеличивать секрецию инсулина и концентрации глюкагона в плазме были сопоставимы. Таким образом, повышенная гликемическая чувствительность к адреналину при диабете 1 типа в значительной степени, возможно, исключительно, является результатом неспособности увеличить секрецию инсулина.
Клиническое влияние HAAF хорошо известно при диабете 1 типа (1,18,29–31).Недавняя предшествующая гипогликемия, даже бессимптомная ночная гипогликемия (29,30), снижает симпатоадреналовый адреналин и нейрогенные симптомы (18,30,31) и ответы когнитивной дисфункции (30,31) на последующую гипогликемию. Он также снижает гликемическую защиту от гиперинсулинемии (18) и снижает выявление гипогликемии в клинических условиях (31). Возможно, наиболее убедительной поддержкой концепции HAAF является открытие трех независимых лабораторий, что всего лишь 2-3 недели скрупулезного избегания ятрогенной гипогликемии обращают вспять отсутствие осведомленности о гипогликемии и улучшают сниженный адреналиновый компонент дефектной контррегуляции глюкозы у большинства больных. (32–35).
Клиническое влияние HAAF менее изучено при диабете 2 типа (1,19). Однако у людей с запущенным (т. Е. С дефицитом инсулина) диабетом 2 типа реакция глюкагона на гипогликемию теряется, как и при диабете 1 типа, и гликемические пороги для реакции адреналина и нейрогенных симптомов смещены в сторону более низких концентраций глюкозы в плазме. недавней предшествующей гипогликемией при диабете 2 типа, как и при диабете 1 типа (19). Таким образом, люди с запущенным сахарным диабетом 2 типа также подвержены риску обоих компонентов HAAF.
В отличие от клинического воздействия HAAF, механизмы HAAF и его фундаментальные компоненты (таблица 1) в значительной степени неизвестны (1). Недавние исследования механизма потери секреторной реакции глюкагона на падение концентрации глюкозы в плазме при инсулино-дефицитном диабете, ключевой особенности синдрома дефектной контррегуляции глюкозы, и исчезновения нейрогенных симптомов гипогликемии, ключевой особенности синдрома неосведомленности о гипогликемии, сначала резюмируются в нижеследующем тексте.Затем обсуждаются исследования потенциальных механизмов сдвига гликемических порогов для симпатоадреналовых ответов на более низкие концентрации глюкозы в плазме, вызванные недавней предшествующей гипогликемией, ключевой особенностью обоих компонентов HAAF.
МЕХАНИЗМ ОТВЕТА ГЛЮКАГОНА НА ГИПОГЛИКЕМИЮ ПРИ ИНСУЛИН-ДЕФИЦИТНОМ ДИАБЕТЕ: ИНСУЛИНОВАЯ ГИПОТЕЗА
О том, что пациенты с диабетом 1 типа не секретируют глюкагон, впервые сообщил Gerich et al.(36) в 1973 г. Потеря секреторной реакции глюкагона на падение концентрации глюкозы в плазме при диабете 1 типа (36,37) и прогрессирующем диабете 2 типа (19) является ключевым признаком нарушения регуляции глюкозы и, таким образом, HAAF (1) . Это выборочный дефект. Ответы глюкагона на другие раздражители в значительной степени, если не полностью, остаются неизменными (38-40). Следовательно, это должна быть сигнальная, а не структурная аномалия α-клеток. Утрата ответа глюкагона тесно коррелирует с потерей секреции эндогенного инсулина (19,41), но не с наличием классической диабетической вегетативной нейропатии (18).Хотя это часто связано с функциональной вегетативной недостаточностью (например, HAAF [1]), у некоторых пациентов с нормальным ответом на адреналин ответ глюкагона отсутствует (37). Ясно, что механизмы этих двух признаков дефектной контррегуляции глюкозы различны.
Признавая, что потеря реакции глюкагона на гипогликемию при инсулино-дефицитном диабете не может быть отнесена к классической диабетической вегетативной нейропатии, Мей и его коллеги (42,43) предположили, что это может быть результатом ранней симпатической нейропатии, которая ограничена. к островкам поджелудочной железы и уникальна для аутоиммунного диабета.Это предположение основано на их обнаружении сниженного маркера симпатических нервных окончаний (переносчик везикулярного моноамина 2) в островках BB, но не у крыс с диабетом, индуцированных стрептозотоцином (42), и сниженных ответов глюкагона на стимуляцию симпатических нервов у крыс с диабетом BB. (43). Очевидно, что этот механизм еще предстоит установить у людей с диабетом 1 типа. Это не объясняет потерю ответа глюкагона при запущенном диабете 2 типа (19). Кроме того, денервированная поджелудочная железа человека (44) и собаки (45) выделяет глюкагон в ответ на гипогликемию.Поэтому мы сосредоточились на ненейронном, периферическом механизме.
Впервые сформулировано Samols et al. (46) и подтвержденная данными исследований перфузируемой поджелудочной железы крыс (47–49), островков крыс (50) и крыс in vivo (51), гипотеза внутриостровкового инсулина утверждает, что снижение секреции инсулина β-клетками и таким образом, снижение уровня инсулина внутри островка и уменьшение тонического ингибирования α-клеток внутри островка инсулином обычно является сигналом к повышенной секреции глюкагона в ответ на гипогликемию.Гипотеза об инсулине внутри островка к настоящему времени подтверждена на людях (10–13). Открытие того, что внутриостровковая гиперинсулинемия, вызванная инфузией толбутамида, стимулирующего секрецию β-клеток, предотвращает реакцию глюкагона на гипогликемию у людей, не страдающих диабетом (10), согласуется с гипотезой, но вполне возможно, что предотвращение ответа глюкагона было результатом внутриостровочная гиперинсулинемия как таковая, а не отсутствие снижения внутриостровкового инсулина. Однако обнаружение того факта, что снижение уровня инсулина внутри островка во время индукции гипогликемии, вызванное подавлением базовой секреции инсулина с помощью АТФ-чувствительного агониста канала K + (канал K ATP ), агониста диазоксида, снижает реакцию глюкагона на гипогликемию ( 11) оказал прямую поддержку гипотезе об инсулине внутри островка.Примечательно, что базальные концентрации глюкагона, быстрый ответ глюкагона на внутривенное введение аргинина и вегетативные (адреномедуллярная, симпатическая и парасимпатическая нервная) реакции на гипогликемию не изменялись диазоксидом. Дополнительные доказательства включают данные о том, что базовое подавление секреции инсулина (и глюкагона) соматостатином, которое устранило снижение уровня инсулина внутри островка во время индукции гипогликемии, снижает ответ глюкагона на гипогликемию (12) и что базовая стимуляция секреции инсулина толбутамидом, который увеличивает снижение уровня инсулина внутри островка во время индукции гипогликемии после отмены толбутамида, увеличивает ответ глюкагона на гипогликемию (13).Таким образом, снижение уровня инсулина внутри островка вместе со снижением уровня глюкозы в α-клетках является сигналом секреторной реакции глюкагона на гипогликемию у здоровых людей. Отсутствие внутриостровкового сигнала инсулина правдоподобно объясняет потерю реакции глюкагона на падение концентрации глюкозы в плазме при эндогенном инсулино-дефицитном (тип 1 [36,37] и прогрессирующий тип 2 [19]) диабет.
МЕХАНИЗМ НЕИЗВЕСТНОСТИ ГИПОГЛИКЕМИИ ПРИ ДИАБЕТЕ: СИМПАТЕТИЧЕСКАЯ НЕЙРОННАЯ ГИПОТЕЗА
Тот факт, что некоторые пациенты с инсулиновым диабетом переносят низкие концентрации глюкозы в плазме с небольшими симптомами, был признан с появлением инсулинотерапии диабета в 1922 году (52), а клинический синдром незнания гипогликемии при диабете (потеря предупреждающих симптомов развития гипогликемии, которые ранее позволяли пациенту распознать и прервать эпизод с помощью еды) был хорошо описан Лоуренсом (53) в середине 20-го века.Незнание гипогликемии или нарушение осведомленности о гипогликемии (более точное описание, поскольку существует диапазон от полного осознания до полного неосведомленности) обычно считалось постоянным долгосрочным осложнением диабета, пока не было обнаружено, что оно обратимо, скрупулезно предотвращение ятрогенной гипогликемии у многих больных через 70 лет после появления инсулинотерапии (32–35).
Симптомы гипогликемии классифицируются как нейрогликопенические, дисфункции головного мозга, обусловленные недостаточностью глюкозы в центральной нервной системе (ЦНС) как таковые, или нейрогенные (54,55).Нейрогенные (или вегетативные) симптомы являются результатом восприятия физиологических изменений, вызванных ЦНС-опосредованными симпатоадреналовыми разрядами, вызванными гипогликемией (55). Они включают как адренергические симптомы (например, учащенное сердцебиение, тремор, возбуждение / беспокойство), опосредованные катехоламинами (норадреналином, адреналином), высвобождаемыми симпатическими постганглионарными нейронами, мозговым веществом надпочечников или и тем, и другим, так и холинергические симптомы (например, потливость, голод, парестезии), опосредованные: ацетилхолин, высвобождаемый симпатическими постганглионарными нейронами (55).Осведомленность о гипогликемии в значительной степени является результатом восприятия нейрогенных, а не нейрогликопенических симптомов у недиабетиков; он снижается не менее чем на 70% при введении антагонистов классических эндогенных вегетативных агонистов (норадреналина, адреналина и ацетилхолина) (55). (Неспособность полностью устранить осведомленность могла быть результатом неполной блокады со стороны конкурирующих антагонистов, дополнительного восприятия нейрогликопенических симптомов или того и другого.Из этого следует, что незнание гипогликемии при диабете должно быть в значительной степени результатом сниженной вегетативной, особенно симпатоадреналовой, активации при данном уровне гипогликемии.
Пациенты с двусторонней адреналэктомией, у которых отсутствует мозговое вещество надпочечников и практически отсутствует реакция адреналина плазмы на гипогликемию, при гипогликемии имеют типичные адренергические и холинергические симптомы (16). Следовательно, нейрогенные симптомы гипогликемии в значительной степени являются результатом активации симпатических нейронов, а не адреномедуллярной, и потеря нейрогенных симптомов у пациентов с диабетом и неосведомленность о гипогликемии должна быть в значительной степени результатом снижения активации симпатических нервов.Интересно, что данные, полученные от пациентов с двусторонней адреналэктомией, также предполагают, что, хотя циркулирующий норадреналин в значительной степени происходит из симпатических нейронов в базальном эвгликемическом состоянии и при некоторых стимулированных условиях, реакция норадреналина плазмы на гипогликемию в значительной степени определяется мозговым веществом надпочечников (16). Кроме того, некоторые гемодинамические реакции (например, увеличение частоты сердечных сокращений и кровотока в предплечье и снижение диастолического артериального давления), по-видимому, в значительной степени опосредованы повышенной адреномедуллярной секрецией адреналина (16).
МЕХАНИЗМ СДВИГА ГЛИКЕМИЧЕСКИХ ПОРОГОВ ДЛЯ СИМПАТОАДРЕНАЛЬНОЙ АКТИВАЦИИ НА НИЖНИЕ КОНЦЕНТРАЦИИ ГЛЮКОЗЫ В ПЛАЗМЕ ПРИ ПОСЛЕДНИХ АНТЕЦЕДЕНТНЫХ ГИПОГЛИКЕМИЯХ
Гипогликемия снижает уровень нейроэндокринных, симптоматических и 29 когнитивных гипогликемий6 58), люди с диабетом 1 типа (18,30,31) и люди с диабетом 2 типа (19). Он сдвигает гликемические пороги этих ответов, включая симпатоадреналовые ответы, на более низкие концентрации глюкозы в плазме.Как обсуждалось ранее, снижение симпатоадреналового ответа на заданный уровень гипогликемии, вызванное недавней предшествующей ятрогенной гипогликемией, играет ключевую роль в патогенезе как дефектной контррегуляции глюкозы (результат сниженных ответов адреналина в условиях отсутствия ответов инсулина и глюкагона), так и незнание гипогликемии (результат снижения нейрогенных симптомов) и, следовательно, HAAF при диабете (1). Механизм или механизмы этого вызванного гипогликемией сдвига гликемических порогов неизвестны.Несколько текущих механистических гипотез обсуждаются ниже.
Помещение ЦНС.
Симпатоадреналовый ответ на гипогликемию, ощущаемый на периферии (например, в воротной вене [59,60] и каротидных телах [61]), а также в переднем и заднем мозге (62), опосредуется через и контролируется ЦНС (1). Обычно считается, что сдвиг гликемических порогов для симпатоадреналовых ответов на более низкие концентрации глюкозы в плазме, вызванный недавней предшествующей гипогликемией, является результатом еще не идентифицированного изменения в ЦНС.Действительно, данные Sivitz et al. (63) можно интерпретировать как снижение прироста активности симпатического нерва надпочечников во время гипогликемии после недавней гипогликемии у крыс в сознании. Тем не менее, снижение симпатоадреналового ответа может быть, по крайней мере частично, результатом изменения на уровне периферических афферентов или эфферентных компонентов симпатоадреналовой системы (64,65). Доказательства последней возможности включают результаты измерений концентраций метанефрина в плазме у людей с диабетом 1 типа (64) и мРНК надпочечников для ферментов биосинтеза катехоламинов у крыс с диабетом, индуцированным стрептозотоцином (65).
Более 90% циркулирующего метанефрина, 0-метилированного метаболита адреналина, происходит из мозгового вещества надпочечников (66). Таким образом, концентрация метанефрина в плазме может быть концептуализирована как отражение адреномедуллярных запасов адреналина и для оценки адреномедуллярной способности секретировать адреналин (66). де Галан и др. (64) обнаружили на ~ 25% более низкие базальные концентрации метанефрина в плазме (а также снижение реакции метанефрина в плазме на гипогликемию) у пациентов с диабетом 1 типа, которые, как известно, имели сниженный ответ адреналина на гипогликемию (и средний уровень HbA 1c 7 .3%). Авторы интерпретировали эти данные как, по общему признанию, косвенное свидетельство снижения адреномедуллярной способности секретировать адреналин у таких пациентов, что является дополнительным компонентом восстановления гликемических порогов. С другой стороны, данные не дают представления о способности выделять норэпинефрин симпатическими постганглионарными нейронами. Концентрации норметанефрина в плазме покоя, 0-метилированного метаболита норэпинефрина, не были снижены у пациентов с диабетом 1 типа (64), но около 30% циркулирующего норметанефрина происходит из мозгового вещества надпочечников, а остальная часть — это результат экстранейрональный метаболизм норадреналина (66).
Inouye et al. (65) обнаружили снижение мРНК тирозингидроксилазы надпочечников (фермент, ограничивающий скорость биосинтеза катехоламинов) на ~ 25% у крыс с индуцированным стрептозотоцином диабетом, но на уровень этого сообщения не повлияла недавняя предшествующая гипогликемия. Напротив, мРНК фенилэтаноламина N -метилтрансферазы надпочечников (фермент, превращающий норадреналин в адреналин) не подвержена влиянию диабета, но снижена на ~ 40% из-за недавней предшествующей гипогликемии. Предполагая, что активность белка фермента биосинтеза катехоламинов и ферментативная активность совпадают с уровнями мРНК и что снижение активности ферментов биосинтеза было достаточным для снижения содержания адреномедуллярных катехоламинов, эти данные согласуются с гипотезой о том, что снижение активности тирозингидроксилазы способствует снижению катехоламиновых ответов. к гипогликемии при диабете и 2 ) пониженная активность фенилэтаноламина N -метилтрансфераза способствует дальнейшему снижению реакции адреналина на гипогликемию после недавней гипогликемии.В качестве альтернативы, как признают авторы, наблюдаемые пониженные уровни мРНК могли быть результатом, а не причиной притупленных катехоламиновых ответов.
Наконец, что касается возможности изменения вне ЦНС, Mevorach et al. (67) предположили, что дополнительный неглюкагон, непинефриновый механизм, возможно, нарушение ауторегуляции глюкозы, может способствовать нарушению контррегуляции глюкозы при диабете 1 типа. Это было основано на их открытии, что снижение концентрации глюкозы в плазме, вызванное низкими дозами инсулина, до 70 мг / дл (3.9 ммоль / л), с фиксированным на исходном уровне глюкагоном и с минимальным повышением уровня адреналина, ассоциировался с примерно на 20% более низкой, частично подавленной инсулином, скоростью выработки эндогенной глюкозы у пациентов с диабетом 1 типа по сравнению с людьми, не страдающими диабетом. Однако, как указали авторы, концентрация адреналина в плазме у пациентов была ниже.
Исходя из предпосылки ЦНС, статус четырех общих гипотез (Таблица 1) относительно изменений ЦНС, которые могут привести к снижению симпатоадреналовой реакции на заданный уровень гипогликемии и, таким образом, объяснить патогенез обоих компонентов HAAF в условиях Отсутствие снижения уровня инсулина и отсутствие прироста глюкагона при инсулино-дефицитном диабете обсуждается ниже.
Гипотеза системного посредника.
Гипотеза системного медиатора утверждает, что повышенные уровни кортизола (или уровни другого системного фактора), стимулированные недавней предшествующей гипогликемией, действуют на мозг, уменьшая симпатоадреналовые ответы на заданный уровень последующей гипогликемии и, таким образом, опосредуют HAAF при инсулино-дефицитном диабете. . Он был сформулирован Дэвисом и др. (68) и подтверждается их выводом о том, что инфузии кортизола (во время эугликемии), как и приступы гипогликемии, снижают адреномедуллярный адреналин и активность мышечной симпатической нервной системы на гипогликемию у здоровых людей на следующий день.(Примечательно, что о влиянии на симптоматические реакции на гипогликемию не сообщалось.) Это было дополнительно подтверждено их выводом о том, что эффект предшествующей гипогликемии не был очевиден у пациентов с первичной адренокортикальной недостаточностью, которые не могли высвобождать кортизол во время предшествующей гипогликемии (69). Общий феномен был подтвержден, когда мы обнаружили, что супрафизиологические уровни кортизола (до ~ 45 мкг / дл), полученные инфузиями фармакологической дозы α 1–24 адренокортикотропного гормона, приводили к снижению адреномедуллярных и нейрогенных симптомов реакции на гипогликемию: день (70).Однако актуальность этого явления для патогенеза HAAF подвергается сомнению. Используя экспериментальную схему, в целом аналогичную той, что первоначально использовалась Davis et al. (68), но при более низких дозах инфузии кортизола, мы обнаружили, что повышение уровня кортизола, сравнимое, а на самом деле несколько выше, такое, которое наблюдается во время гипогликемии (~ 26 мкг / дл), не снижает адреномедуллярную или нейрогенную реакцию симптомов на гипогликемию на следующий день у здоровых людей. частные лица (71). Более того, ответ на глюкокортикоиды коры надпочечников, по-видимому, не имеет решающего значения для эффекта предшествующей гипогликемии.Несмотря на отсутствие реакции кортикостерона на гипогликемию, недавняя предшествующая гипогликемия снижала ответы адреналина и глюкагона на последующую гипогликемию у мышей с нокаутом кортикотропин-рилизинг-гормона (72). Таким образом, ответ кортизола на предшествующую гипогликемию, по-видимому, не является медиатором HAAF.
Несмотря на очевидное, хотя и фармакологическое, подтверждение этого феномена у людей (70), влияние центральных глюкокортикоидов на снижение симпатоадреналовой реакции на последующую гипогликемию у грызунов остается спорным.Сообщалось, что кортикостерон, вводимый подкожно (73), внутривенно (74) или в третий желудочек головного мозга (75), не снижает симпатоадреналовый ответ на гипогликемию, тогда как кортизол, вводимый в боковой желудочек головного мозга (76), и дексаметазон, вводимый периферически или в четвертый желудочек головного мозга (но не третий желудочек головного мозга) (77), как сообщается, снижает эту реакцию.
Имеются также данные о том, что недавнее предшествующее повышение уровня адреналина не вызывает HAAF (78).Инфузии адреналина не снижали плазменный адреналин (или глюкагон) и нейрогенные симтомные реакции на последующую гипогликемию у недиабетических субъектов.
Гипотеза транспорта топлива для мозга.
Гипотеза о транспортировке топлива в мозг утверждает, что недавняя предшествующая гипогликемия увеличивает транспорт глюкозы из крови в мозг (или транспорта альтернативных видов топлива) за счет активации транспортеров гематоэнцефалического барьера и что усиление транспорта топлива в мозг снижает ответы, в том числе симпатоадреналовые реакции, на последующая гипогликемия и, следовательно, является механизмом HAAF.Он основан на значительном количестве данных на грызунах, указывающих на то, что гипогликемия ≥3 дней (не часов) увеличивает мРНК GLUT-1 микрососудов мозга и поглощение белка и глюкозы в мозге (79–83). Однако актуальность этих данных для HAAF сомнительна, поскольку феномен HAAF может быть вызван несколькими часами предшествующей гипогликемии у людей (56-58).
Boyle et al. (84) обнаружили, что поглощение глюкозы головным мозгом (рассчитанное на основе артериовенозных различий глюкозы в мозговых и церебральных кровотоках; метод Кети-Шмидта) сохраняется во время гипогликемии после ~ 56 часов межпрандиальной гипогликемии у здоровых людей и у пациентов с хорошо -управляемый (т.е., часто гипогликемический) диабет 1 типа (85). И снова, однако, актуальность первого открытия для HAAF сомнительна, учитывая, что оно было продемонстрировано только после> 2 дней гипогликемии. С другой стороны, гипотеза транспорта глюкозы в головном мозге была непосредственно проверена на модели HAAF (86) и на пациентах с диабетом 1 типа с гипогликемией и без нее (87). Что касается модели, используя [1- 11 C] глюкозы и позитронно-эмиссионную томографию (ПЭТ), мы обнаружили, что глобальный транспорт глюкозы от крови к мозгу не увеличивался после ~ 24 часов межпрандиальной гипогликемии (которая снижала симпатоадреналовый синдром). и нейрогенные симптомы симптомов в ответ на гипогликемию существенно) у здоровых субъектов (86).У пациентов с диабетом 1 типа Bingham et al. (87) не обнаружили различий в глобальном транспорте глюкозы из крови в мозг, измеренном с помощью [ 11 C] 3–0-метилглюкозы и ПЭТ, между пациентами с гипогликемией и без нее. Эти данные не исключают увеличения регионального транспорта глюкозы из крови в мозг, но, как обсуждалось выше, гипотеза была основана на доказательствах увеличения глобального транспорта глюкозы у грызунов (79–83) и человека (84,85). Кроме того, у грызунов краткосрочная предшествующая гипогликемия, которая снижает симпатоадреналовые ответы на последующую гипогликемию, как это происходит у людей, не увеличивает региональные концентрации внеклеточной глюкозы в мозге, как измерено с помощью микродиализа в вентромедиальном гипоталамусе (ВМГ) (88). ствол мозга (89) или гиппокамп (90) во время последующей гипогликемии.Действительно, у людей недавняя предшествующая гипогликемия не приводила к значительному увеличению концентрации глюкозы в головном мозге, измеренной с помощью спектроскопии ядерного магнитного резонанса, во время последующей гипогликемии (91).
Таким образом, накапливающиеся доказательства не подтверждают мнение о том, что усиление транспорта глюкозы из крови в мозг является механизмом HAAF. Тем не менее, обнаружение немного более высоких концентраций глюкозы в головном мозге (в среднем 5,5 мкмоль / г по сравнению с 4,7 мкмоль / г у недиабетиков), измеренных с помощью ядерного магнитного резонанса во время значительной гипергликемии, у пациентов с строго контролируемым диабетом 1 типа и вероятной неосведомленностью о гипогликемии (92) можно интерпретировать как совместимое с гипотезой.Однако, используя тот же метод и те же гипергликемические состояния, в отдельном исследовании эти исследователи сообщили о средней концентрации глюкозы в головном мозге 5,3 мкмоль / г у недиабетиков (незначительно отличается от 4,7 мкмоль / г у пациентов с плохо контролируемым типом). 1 сахарный диабет) (93). Кроме того, используя [ 11 C] 3-0-метилглюкозу и ПЭТ, Bingham et al. (87) не обнаружили различий в содержании глюкозы в мозге у пациентов с гипогликемией и без нее.
Увеличение транспорта топлива, отличного от глюкозы, в мозг теоретически может объяснить HAAF.В связи с этим Mason et al. (94) представили доказательства увеличения транспорта ацетата из крови в мозг у пациентов с диабетом 1 типа, что повышает вероятность того, что усиленный транспорт монокарбоксилата (например, лактата) из крови в мозг может быть механизмом HAAF. Очевидно, что последнее еще предстоит напрямую продемонстрировать и показать, что он специфичен для пациентов с неосведомленностью о гипогликемии.
Гипотеза метаболизма мозга.
Гипотеза метаболизма головного мозга предполагает, что недавняя предшествующая гипогликемия каким-то образом изменяет метаболизм мозга, что в конечном итоге приводит к снижению опосредованных ЦНС ответов, включая симпатоадреналовые реакции, на последующую гипогликемию.Большая часть исследований патогенеза HAAF при диабете сосредоточена на VMH (95). Глюкопения VMH (введение 2-дезоксиглюкозы) активирует симпатоадреналовую систему и увеличивает секрецию глюкагона (96), а перфузия глюкозы VMH подавляет эти реакции во время системной гипогликемии (97). Тем не менее, активация контррегуляторных систем глюкозы затрагивает обширные области мозга у экспериментальных животных (98,99) и людей (100,101).
Мы использовали [ 15 0] воду и ПЭТ для измерения регионального церебрального кровотока, маркера синаптической активации, во время гипогликемии у здоровых людей (100).Одним из новых открытий было небольшое (6-8%) генерализованное (например, головной мозг, ствол мозга и мозжечок) снижение мозгового кровотока с более выраженным снижением (25%) в гиппокампе, что может отражать снижение метаболизма мозга из-за недостатку глюкозы и уязвимости гиппокампа. С другой стороны, типичные симпатоадреналовые и симптоматические реакции на гипогликемию были связаны с синаптической активацией в широко распространенных, но дискретных областях мозга, включая медиальную префронтальную кору, еще одно новое открытие, а также таламус и периакведуктальный серый цвет.(Эти данные вроде бы подтвердились [101]). Медиальная префронтальная кора и ее связи обеспечивают основной корковый выход вегетативным структурам в гипоталамусе и периакведуктальном сером (100, 102). Эти данные открывают возможность корковой модуляции симпатоадреналового ответа на простой физиологический процесс низкого уровня: защиту от гипогликемии. По крайней мере, они указывают на то, что при изучении механизмов HAAF в ЦНС при диабете необходимо учитывать широко распространенные области мозга.Эти данные свидетельствуют о том, что метаболические изменения, вызванные недавней предшествующей гипогликемией и приводящие к изменению синаптической активности во время последующей гипогликемии, происходят в обширных областях мозга, включая кору, и могут быть вовлечены в патогенез HAAF при диабете. Интересно, что Tkacs et al. (103) обнаружили доказательства клеточной (предположительно нейрональной) гибели в ростральных областях мозга, включая медиальную префронтальную кору (но не в гиппокампе), что было связано со сниженным ответом адреналина на гипогликемию у крыс, подвергшихся воздействию глюкозы в плазме 30–30%. 35 мг / дл на 75 мин 48 ч назад.Примечательно, что доказательства клеточной смерти мозга не были обнаружены после уровней глюкозы ~ 45 мг / дл.
Существует множество возможных изменений метаболизма мозга, которые могут быть механизмом HAAF, но ни одно из них не установлено однозначно. Одна из возможностей состоит в том, что недавняя предшествующая гипогликемия приводит к увеличению активности глюкокиназы в критических, возможно, VMH, глюкозо-чувствительных нейронах, которые запускают симпатоадреналовый ответ (95,104-106). Ожидается, что результирующий повышенный нейрональный метаболизм глюкозы приведет к снижению симпатоадреналовой реакции на заданный уровень последующей гипогликемии.Экспрессия глюкокиназы (и GLUT-2) была продемонстрирована в головном мозге человека, в том числе в VMH (дугообразное ядро и вентромедиальное ядро гипоталамуса) (107). Интересно, что инфузия фруктозы, которая может модулировать активность глюкокиназы в соответствующих центральных нейронах, почти нормализует реакцию плазменного адреналина (но не реакцию глюкагона) на гипогликемию у пациентов с диабетом 1 типа (108). Многие другие изменения в передаче сигналов или метаболизме мозга могут вносить вклад в патогенез HAAF.К ним относятся повышенное высвобождение кортикотропин-рилизинг-гормона или урокортина (73,109), снижение активности паравентрикулярного ядра гипоталамуса (75,110,111), закрытие канала K ATP (112,113), снижение активности гипоталамической AMP-активируемой протеинкиназы (114–116), повышение ГАМКергического тонуса. (117,118), усиление гипоталамической экспрессии ангиотензиногена и родственных генов (119), снижение церебрального метаболизма глюкозы (87), увеличение мозгового кровотока (120) и снижение передачи сигналов инсулина в головном мозге (121, 122).Интересно, что Bingham et al. (87), используя [ 11 C] 3-0-метилглюкозу и ПЭТ, обнаружили относительное снижение церебрального метаболизма глюкозы во время гипогликемии у небольшой выборки пациентов с диабетом 1 типа и не осознающих гипогликемию. Церебральный метаболизм глюкозы имел тенденцию увеличиваться у осведомленных пациентов, но снижался у неосведомленных пациентов, что приводило к значительно более низкой средней скорости метаболизма глюкозы у последних. Однако, используя [1- 11 C] глюкозу и ПЭТ, мы не обнаружили различий в метаболизме церебральной глюкозы во время неосведомленности о гипогликемии, вызванной недавней предшествующей гипогликемией у недиабетических лиц (86).
Гипотеза суперкомпенсации гликогена в мозге.
Гипотеза суперкомпенсации гликогена в мозге утверждает, что после эпизода гипогликемии уровни гликогена в головном мозге (астроцитах) восстанавливаются до уровней, превышающих предгипогликемические концентрации, и обеспечивают расширенный источник гликолитического и, в конечном итоге, окислительного топлива нейронов (например, лактата), что объясняет снижение симпатоадреналовый ответ на заданный уровень последующей гипогликемии (123). Он основан на данных на крысах, показывающих, что концентрации гликогена в мозге несколько выше, чем сообщалось ранее (124), и что концентрации гликогена в мозге, измеренные с помощью спектроскопии ядерного магнитного резонанса, снижаются во время гипогликемии, но затем увеличиваются до ~ 150% от базальных уровней> 7. ч после восстановления эугликемии (125).Кроме того, сообщалось, что обмен гликогена в человеческом мозге относительно медленный (125,126). Очевидно, что феномен суперкомпенсации имеет решающее значение для этой гипотезы, поскольку, даже с учетом обновленных оценок, содержание гликогена в мозге на несколько порядков ниже, чем содержание гликогена в печени и мышцах, гликоген в мозге падает с полупериодом в несколько минут в течение глобального периода. ишемия, а обмен гликогена в головном мозге составляет несколько процентов от потребления глюкозы, как измерено у крыс (127).
РАЗЛИЧНЫЕ ПРИЧИНЫ HAAF ПРИ ДИАБЕТЕ
Первоначально мы связывали HAAF при диабете исключительно с недавней антецедентной ятрогенной гипогликемией (18,19).Однако вполне может быть, что предшествующие события в дополнение к гипогликемии вызывают феномен HAAF (1) (рис. 1).
Было обнаружено, что предшествующие упражнения снижают симпатоадреналовый ответ на последующую гипогликемию (128,129). Галассетти и др. (128) обнаружили, что физические упражнения снижают активность адреналина и мышечных симпатических нервов, но не вызывают нейрогенные симптомы, а именно реакцию на последующую гипогликемию. Мы также обнаружили, что предшествующие упражнения снижали реакцию адреналина на последующую гипогликемию (129).И снова, однако, реакции нейрогенных симптомов на гипогликемию не уменьшились. Таким образом, поскольку предшествующие упражнения не уменьшают симптомы, то есть не вызывают гипогликемии, связанный с физической нагрузкой HAAF, по-видимому, является частичным синдромом HAAF.
HAAF, связанный со сном, — более убедительный пример. У людей с сахарным диабетом 1 типа значительно снижены симпатоадреналовые реакции на определенный уровень гипогликемии, и их симпатоадреналовые ответы еще больше снижаются во время сна (130, 131). Вероятно, из-за заметно сниженного симпатоадреналового ответа (132) люди с диабетом 1 типа гораздо реже просыпаются от сна из-за гипогликемии, чем люди, не страдающие диабетом (131).Во время гипогликемии они спали примерно 75–80% времени, тогда как контрольные субъекты без диабета спали только примерно 25% времени (131). Таким образом, у спящих пациентов с сахарным диабетом 1 типа наблюдается как нарушение регуляции глюкозы (дальнейшее снижение реакции адреналина в условиях отсутствия ответов на инсулин и глюкагон), так и форма неосведомленности о гипогликемии (снижение возбуждения от сна), два компонента HAAF при диабете ( 1).
Таким образом, существуют различные причины HAAF при диабете: первоначально выявленные HAAF, связанные с гипогликемией, HAAF, связанные с физической нагрузкой, и HAAF, связанные со сном (1).Ясно, что объединяющий механизм HAAF должен включать эффекты предшествующей гипогликемии, предшествующих физических упражнений и сна.
КОММЕНТАРИЙ
У многих пациентов с диабетом возможно как снизить риск гипогликемии, так и улучшить гликемический контроль (1, 233, 134). Тем не менее ятрогенная гипогликемия продолжает оставаться проблемой для людей с диабетом, которая не решена. В ожидании профилактики и лечения диабета необходимы критически важные фундаментальные, трансляционные исследования и исследования результатов, если мы хотим устранить гипогликемию из жизни людей, страдающих диабетом.
РИС. 1.Автономная недостаточность, связанная с гипогликемией, при диабете 1 типа. Изменено из исх. 1. © 2004 Медицинское общество MA.
ТАБЛИЦА 1Механизмы основных компонентов вегетативной недостаточности, связанной с гипогликемией, при диабете
Благодарности
Цитируемая автором работа была частично поддержана Службой общественного здравоохранения США / Национальным институтом здравоохранения, гранты R37 DK27085, M01 RR00036 и P60 DK20579 и стипендией Американской диабетической ассоциации.
Автор с благодарностью отмечает существенный вклад своих докторантов и сотрудников, а также квалифицированную помощь медперсонала и технического персонала Университета Вашингтонского Университета в проведении наших исследований и Джанет Дедеке в подготовке этой рукописи.
Сноски
- Принята 8 августа 2005 г.
- Получена 28 июня 2005 г.
- ДИАБЕТ
СПРАВОЧНЫЕ МАТЕРИАЛЫ
- ↵
Крайер PE: Диабет, связанный с гипогликемией. .N Engl J Med350 : 2272 –2279,2004
- ↵
Hirsch IB: аналоги инсулина. N Engl J Med352 : 174 –183,2005
- ↵
Группа по исследованию контроля диабета и его осложнений: Влияние интенсивного лечения диабета на развитие и прогрессирование отдаленных осложнений инсулинозависимого сахарного диабета. N Engl J Med329 : 977 –986,1993
- ↵
Группа перспективного исследования диабета в Великобритании (UKPDS): Интенсивный контроль уровня глюкозы в крови с помощью сульфонилмочевины или инсулина по сравнению с традиционным лечением и риск осложнений у пациентов с диабетом 2 типа (UKPDS 33).Ланцет352 : 837 –853,1998
- ↵
Группа перспективного исследования диабета в Великобритании (UKPDS): влияние интенсивного контроля уровня глюкозы в крови с помощью метформина на осложнения у пациентов с избыточной массой тела и диабетом 2 типа (UKPDS 34). Ланцет352 : 854 –865,1998
- ↵
Bulsara MK, Holman CDJ, Davis EA, Jones TW: Влияние десятилетнего изменения лечения на частоту тяжелой гипогликемии в популяционной когорте детей с диабетом 1 типа. Уход за диабетом27 : 2293 –2298,2004
- ↵
Holstein A, Plaschke A, Egberts E-H: Клиническая характеристика тяжелой гипогликемии: проспективное популяционное исследование.Exp Clin Endocrinol Diabetes111 : 364 –369,2003
- ↵
Leese GP, Wang J, Broomhall J, Kelly P, Marsden A, Morrison W., Frier BM, Morris AD, DARTS / MEMO Collaboration: Частота тяжелой гипогликемии, требующей неотложной помощи. Сахарный диабет 1 и 2 типа: популяционное исследование использования ресурсов здравоохранения. Уход за диабетом26 : 1176 –1180,2003
- ↵
Cryer PE: Профилактика и коррекция гипогликемии. В Справочник по физиологии.Раздел 7: Эндокринная система. Том II: Эндокринная поджелудочная железа и регуляция метаболизма. Джефферсон LS, Черрингтон AD, Eds. Нью-Йорк, Oxford University Press, 2001. , стр.1057 –1092
- ↵
Банарер С., МакГрегор В.П., Крайер П.Е .: Внутриплеточная гиперинсулинемия предотвращает реакцию глюкагона на гипогликемию, несмотря на сохранность вегетативной реакции. Диабет51 : 958 –965,2002
- ↵
Раджу Б., Крайер П.Е .: Потеря декремента внутриостровкового инсулина правдоподобно объясняет потерю реакции глюкагона на гипогликемию при инсулино-дефицитном диабете.Диабет54 : 757 –764,2005
- ↵
Госманов Н.Р., Сокэ Э., Исраэлиан З., Смит Т., Крайер П.Е., Герих Дж. Э., Мейер С. Роль декремента внутрижелкового инсулина в ответе глюкагона на гипогликемию у людей. Уход за диабетом28 : 1124 –1131,2005
- ↵
Исраэлян З., Госманов Н.Р., Шоке Э., Бохари С., Крайер П.Е., Герич Дж. Э., Мейер К. Увеличение снижения секреции инсулина улучшает реакцию глюкагона на гипогликемию при запущенном диабете 2 типа.Уход за диабетом28 : 2691 –2696,2005
- ↵
White NH, Skor DA, Cryer PE, Levandoski LA, Bier DM, Santiago JV: Выявление пациентов с диабетом 1 типа с повышенным риском гипогликемии во время интенсивной терапии. N Engl J Med308 : 485 –491,1983
- ↵
Bolli GB, De Feo P, De Cosmo S, Perriello G, Ventura MM, Benedetti MM, Santeusanio F, Gerich JE, Brunetti P: надежный и воспроизводимый тест для адекватной контррегуляции глюкозы в сахарный диабет 1 типа.Диабет33 : 732 –737,1984
- ↵
ДеРоса М.А., Крайер П.Е .: Гипогликемия и симпатоадреналовая система: нейрогенные симптомы в значительной степени являются результатом симпатической нервной, а не адреномедуллярной активации. Am J Physiol Endocrinol Metab287 : E32 –E41,2004
- ↵
Gold AE, MacLeod KM, Frier BM: Частота тяжелой гипогликемии у пациентов с диабетом 1 типа с нарушением осведомленности о гипогликемии. Уход за диабетом17 : 697 –703,1994
- ↵
Дагого-Джек С.Е., Крафт С., Крайер П.Е .: Автономная недостаточность, связанная с гипогликемией, при инсулинозависимом сахарном диабете.J Clin Invest91 : 819 –828,1993
- ↵
Сегель С.А., Парамор Д.С., Крайер PE: вегетативная недостаточность, связанная с гипогликемией, при запущенном диабете 2 типа. Диабет51 : 724 –733,2002
- ↵
Berk MA, Clutter WE, Skor D, Shah SD, Gingerich RP, Parvin CA, Cryer PE: Повышенная гликемическая реакция на эпинефрин при инсулинозависимом сахарном диабете является результатом неспособности выделяют инсулин. J Clin Invest75 : 1842 –1851,1985
- ↵
Диверти Г.Д., Дженсен М.Д., Крайер П.Е., Майлз Дж. М.: Липолитическая реакция на адреналин у людей без диабета и диабета.Am J Physiol Endocrinol Metab272 : E1130 –E1135,1997
- ↵
Enoksson S, Caprio S, Rife F, Shulman GI, Tamborlane WV, Sherwin RS: Дефектная активация липолиза скелетных мышц и жировой ткани при сахарном диабете 1 типа во время гипогликемии. J Clin Endocrinol Metab88 : 1503 –1511,2003
- ↵
Berlin I, Grimaldi A, Landault C, Zoghbi F, Thervet F, Puech AJ, Legrand JC: Отсутствие гипогликемических симптомов и снижение β-адренергической чувствительности у пациентов с инсулинозависимым диабетом.J Clin Endocrinol Metab66 : 273 –278,1988
- ↵
Корытковски М.Т., Мокан М., Венеман Т.Ф., Митраку А., Крайер П.Е., Герич Дж. Э .: Снижение β-адренергической чувствительности у пациентов с сахарным диабетом 1 типа и гипогликемией. Уход за диабетом21 : 1939 –1943,1998
- ↵
Фриче А., Стефан Н., Херинг Х, Герих Дж., Штумволл М.: Предотвращение гипогликемии восстанавливает осведомленность о гипогликемии за счет повышения β-адренергической чувствительности при диабете 1 типа. Энн Интерн Мед134 : 729 –736,2001
- ↵
Fritsche A, Stumvoll M, Grüb M, Sieslack S, Renn W., Schmülling RM, Häring HU, Gerich JE: Влияние гипогликемии на β-адренергическую чувствительность у нормальных субъектов и пациентов с диабетом 1 типа .Уход за диабетом21 : 1505 –1510,1998
- ↵
de Galan BE, de Mol P, Wennekes L, Tack CJ, Smits P: β 2 -адренергическая чувствительность не снижается у пациентов с диабетом 1 типа с неосведомленностью о гипогликемии (Аннотация). Диабет53 (Приложение 2) : A164 , 2004
- ↵
Афтаб Гай Д., Сандовал Д., Ричардсон М.А., Тейт Д., Флаколл П.Дж., Дэвис С.Н.: Различные физиологические эффекты адреналина при диабете 1 типа и недиабетических людях. Am J Physiol Endocrinol Metab288 : E178 –E186,2005
- ↵
Венеман Т., Митраку А., Мокан М., Крайер П., Герич Дж.: Вызвание неосведомленности о гипогликемии бессимптомной ночной гипогликемией.Диабет42 : 1233 –1237,1993
- ↵
Fanelli CG, Paramore DS, Hershey T, Terkamp C, Ovalle F, Craft S, Cryer PE: Влияние ночной гипогликемии на гипогликемическую когнитивную дисфункцию при диабете 1 типа. Диабет47 : 1920 –1927,1998
- ↵
Ovalle F, Fanelli CG, Paramore DS, Craft S, Cryer PE: Краткие два раза в неделю эпизоды гипогликемии снижают вероятность выявления клинической гипогликемии при сахарном диабете 1 типа. Диабет47 : 1472 –1479,1998
- ↵
Fanelli CG, Epifano L, Rambotti AM, Pampanelli S, Di Vincenzo A, Modarelli F, Lepore M, Annibale B, Ciofetta M, Bottini P, Porcellati F, Scionti L, Santeus , Брунетти П., Болли Г.Б.: Тщательная профилактика гипогликемии нормализует гликемические пороги и величину большинства нейроэндокринных реакций, симптомов и когнитивных функций во время гипогликемии у интенсивно леченных пациентов с краткосрочным ИЗСД.Диабет42 : 1683 –1689,1993
Крэнстон И., Ломас Дж., Маран А., Макдональд И., Амиэль С.А.: Восстановление осведомленности о гипогликемии у пациентов с длительным инсулинозависимым диабетом. Ланцет344 : 283 –287,1994
Fanelli C, Pampanelli S, Epifano L, Rambotti AM, Di Vincenzo A, Modarelli F, Ciofetta M, Lepore M, Annibale B, Torlone E, Perriello G, De Feo P, Santeusanio F , Брунетти П., Болли Г.Б.: Долгосрочное выздоровление от неосведомленности, недостаточной контррегуляции и отсутствия когнитивной дисфункции во время гипогликемии после введения рациональной интенсивной инсулиновой терапии при ИЗСД.Диабетология37 : 1265 –1276,1994
- ↵
Дагого-Джек С., Раттарасарн С., Крайер П.Е .: Устранение неосведомленности о гипогликемии, но не нарушения регуляции глюкозы при IDDM. Диабет43 : 1426 –1434,1994
- ↵
Gerich JE, Langlois M, Noacco C, Karam JH, Forsham PH: Отсутствие реакции глюкагона на гипогликемию при диабете: свидетельства внутреннего дефекта альфа-клеток поджелудочной железы. Наука182 : 171 –173,1973
- ↵
Bolli G, De Feo P, Compagnucci P, Cartechini MG, Angeletti F, Santeusanio F, Brunetti P, Gerich JE: Аномальная контррегуляция глюкозы при инсулинозависимом сахарном диабете: взаимодействие антиинсулинов антитела и нарушение секреции глюкагона и адреналина.Диабет32 : 134 –141,1983
- ↵
Wiethop BV, Cryer PE: Гликемическое действие аланина и тербуталина при IDDM. Уход за диабетом16 : 1124 –1130,1993
Caprio S, Tamborlane WV, Zych K, Gerow K, Sherwin RS: Утрата потенцирующего эффекта гипогликемии на реакцию глюкагона на гипераминоацидемию при IDDM. Диабет42 : 550 –555,1993
- ↵
Hoffman RP, Singer-Granick C, Drash AL, Becker DJ: Аномальное распознавание гипогликемии альфа-клетками у детей с инсулинозависимым сахарным диабетом (IDDM).J Педиатр Эндокринол7 : 225 –234,1994
- ↵
Фукуда М., Танака А., Тахар Ю., Икегами Х., Ямамото Ю., Кумахара Ю., Шима К. Корреляция между минимальной секреторной способностью β-клеток поджелудочной железы и стабильностью контроля диабета. Сахарный диабет37 : 81 –88,1988
- ↵
Mei Q, Mundinger TO, Lernmark A, Taborsky GJ Jr: Ранняя, избирательная и заметная потеря симпатических нервов с островков у диабетических крыс BioBreeder. Диабет51 : 2997 –3002,2002
- ↵
Mundinger TO, Mei Q, Figlewicz DP, Lernmark A, Taborsky GJ Jr: Нарушение реакции глюкагона на стимуляцию симпатического нерва у диабетической крысы BB: эффект ранней симпатической островковой невропатии.Am J Physiol Endocrinol Metab285 : E1047 –E1054,2003
- ↵
Diem P, Redmon JB, Abid M, Moran A, Sutherland DER, Halter JB, Robertson RP: секреция глюкагона, катехоламинов и панкреатических полипептидов у реципиентов аллотрансплантатов поджелудочной железы у больных диабетом 1 типа. J Clin Invest86 : 2008 –2013,1990
- ↵
Sherck SM, Shiota M, Saccomando J, Cardin S, Allen EJ, Hastings JR, Neal DW, Williams PE, Cherrington AD: панкреатическая реакция на умеренную неинсулино-индуцированную гипогликемию не проявляется. вовлекают внешние нервные импульсы.Диабет50 : 2487 –2496,2001
- ↵
Самолс Э., Тайлер Дж., Маркс В. Взаимосвязь глюкагона и инсулина. В Глюкагон: молекулярная физиология, клинические и терапевтические последствия. Лефевр П., Унгер Р. Х., ред. Элмсфорд, штат Нью-Йорк, Пергамон, стр.151. –174,1972
- ↵
Samols E, Stagner JI, Ewart RBL, Marks V: Порядок перфузии островковых микрососудистых клеток: B → A → D в перфузируемой поджелудочной железе крысы. J Clin Invest82 : 350 –353,1988
Маруяма Х., Хисатони А., Орчи Л., Гродский Г.М., Унгер Р.Х.: Инсулин внутри островков является физиологическим ингибитором высвобождения глюкагона.J Clin Invest74 : 2296 –2299,1984
- ↵
Мокуда О., Шибата М., Оока Х., Окадзаки Р., Сакамото Ю. Глюкагон парадоксальным образом секретируется при высоких концентрациях глюкозы в поджелудочной железе крысы, перфузированной диазоксидом. Диабет Нутр Метаб15 : 260 –264,2002
- ↵
Hope KM, Tran POT, Zhou H, Oseid E, LeRoy E, Robertson RP: Регулирование функции α-клеток β-клетками в изолированных островках человека и крысы, лишенных глюкозы: гипотеза «выключения».Диабет53 : 1488 –1495,2004
- ↵
Zhou H, Tran POT, Yang S, Zhang T, LeRoy E, Oseid E, Robertson RP: Регулирование функции α-клеток β-клетками во время гипогликемии у крыс Wistar: Гипотеза «выключения». Диабет53 : 1482 –1487,2004
- ↵
Флетчер А.А., Кэмпбелл В.Р.: Уровень сахара в крови после введения инсулина и комплекс симптомов: гипогликемия. J Metab Res2 : 637 –649,1922
- ↵
Лоуренс РД: Инсулиновая гипогликемия: изменения нервных проявлений.Lancetii : 602 , 1941
- ↵
Deary IJ, Hepburn DA, MacLeod KM, Frier BM: Разделение симптомов гипогликемии с использованием многоэлементного анализа факторов подтверждения. Диабетология36 : 771 –777,1993
- ↵
Towler DA, Havlin CE, Craft S, Cryer PE: Механизм осознания гипогликемии: восприятие нейрогенных (преимущественно холинергических), а не нейрогликопенических симптомов. Диабет42 : 1791 –1798,1993
- ↵
Heller SR, Cryer PE: Снижение нейроэндокринных и симптоматических реакций на последующую гипогликемию после одного эпизода гипогликемии у недиабетических людей.Диабет40 : 223 –226,1991
Дэвис М., Шамун Х: Противорегулирующая адаптация к рецидивирующей гипогликемии у нормальных людей. J Clin Endocrinol Metab73 : 995 –1001,1991
- ↵
Дэвис С.Н., Шейверс С., Москеда-Гарсиа, Коста Ф: Влияние различных предшествующих гипогликемий на последующую контррегуляцию у нормальных людей. Диабет46 : 1328 –1335,1997
- ↵
Хевенер А.Л., Бергман Р.Н., Донован К.М.: Афференты воротной вены имеют решающее значение для симпатоадреналовой реакции на гипогликемию.Диабет49 : 8 –12,2000
- ↵
Smith D, Pernet A, Reid H, Bingham E, Rosenthal JM, Macdonald I, Umpleby AM, Amiel SA: Роль определения глюкозы в воротной вене печени в модулировании реакции на гипогликемию у человека. Диабетология45 : 1416 –1424,2002
- ↵
Koyama Y, Coker RH, Stone EE, Lacy DB, Jabbour K, Williams PE, Wasserman DH: Доказательства того, что каротидные тела играют важную роль в глюкорегуляции in vivo. Диабет49 : 1434 –1442,2000
- ↵
Frizzell RT, Jones EM, Davis SN, Biggers DW, Myers SR, Connolly CC, Neal DW, Jaspan JB, Cherrington AD: Контррегуляция во время гипогликемии направляется широко распространенными областями мозга.Диабет42 : 1253 –1261,1993
- ↵
Сивитц В.И., Херлейн И.А., Морган Д.А., Финк Б.Д., Филлипс Б.Г., Хейнс В.Г .: Влияние острой и предшествующей гипогликемии на симпатическую нервную активность и реакцию на катехоламины у нормальных крыс. Диабет50 : 1119 –1125,2001
- ↵
de Galan BE, Tack CJ, Willemsen JJ, Sweep CGJ, Smits P, Lenders JWM: уровни метанефрина в плазме снижены у пациентов с диабетом 1 типа с тяжелым нарушением реакции эпинефрина на гипогликемию, что указывает на снижение адреномедуллярных запасов адреналина.J Clin Endocrinol Metab89 : 2057 –2061,2004
- ↵
Inouye KE, Chan O, Yue JTY, Matthews SG, Vranic M: Влияние диабета и рецидивирующей гипогликемии на регуляцию симпатоадреналовой системы и гипоталамо-гипофизарно-надпочечниковой системы. Am J Physiol Endocrinol Metab288 : E422 –E429,2005
- ↵
Eisenhofer G, Kopin IJ, Goldstein DS: Метаболизм катехоламинов: современный взгляд на физиологию и медицину. Pharmacol Rev56 : 331 –349,2004
- ↵
Mevorach M, Kaplan J, Chang CJ, Rossetti L., Shamoon H: Гормононезависимая активация EGP во время гипогликемии отсутствует при сахарном диабете 1 типа.Am J Physiol Endocrinol Metab278 : E421 –E429,2000
- ↵
Дэвис С.Н., Шейверс С., Коста Ф, Москеда-Гарсия Р.: Роль кортизола в патогенезе недостаточной контррегуляции после предшествующей гипогликемии у нормальных людей. J Clin Invest98 : 680 –691,1996
- ↵
Дэвис С.Н., Шейверс С., Дэвис Б., Коста Ф .: Предотвращение повышения уровня кортизола в плазме во время гипогликемии позволяет сохранить последующие контррегуляторные реакции. J Clin Invest100 : 429 –438,1997
- ↵
McGregor VP, Banarer S, Cryer PE: Повышенный уровень эндогенного кортизола снижает вегетативную нейроэндокринную реакцию и реакцию симптомов на последующую гипогликемию.Am J Physiol Endocrinol Metab282 : E770 –E777,2002
- ↵
Раджу Б., МакГрегор В.П., Крайер П.Е .: Повышение уровня кортизола, сравнимое с тем, которое происходит при гипогликемии, не вызывает вегетативной недостаточности, связанной с гипогликемией. Диабет52 : 2083 –2089,2003
- ↵
McGuinness O, Ansari T, Potts J, Jacobson L: Глюкокортикоидная недостаточность у мышей с нокаутом высвобождающего кортикотропина не сохраняет вегетативные реакции во время повторных зажимов гипогликемии (Аннотация).Диабет54 (Приложение 1) : A26 , 2005
- ↵
Flanagan DE, Keshavarz T, Evans ML, Flanagan S, Fan X, Jacob RJ, Sherwin RS: Роль кортикотропин-рилизинг-гормона в нарушении контррегуляторных реакций на гипогликемию. Диабет52 : 605 –613,2003
- ↵
Шум К., Иноуэ К., Чан О, Матху Дж., Билински Д., Мэтьюз С.Г., Вранич М.: Влияние предшествующей гипогликемии, гиперинсулинемии и избытка кортикостерона на контррегуляцию гипогликемии.Am J Physiol Endocrinol Metab281 : E455 –E465,2001
- ↵
Evans SB, Wilkinson CW, Bentson K, Gronbeck P, Zavosh A, Figlewicz DP: активация PVN подавляется повторной гипогликемией, но не предшествующим кортикостероном у крыс. Am J Physiol Regul Integr Comp Physiol281 : R1426 –R1436,2001
- ↵
Сандовал Д., Пинг Л., Нил А.Р., Морри С., Дэвис С.Н.: Кортизол действует через центральные механизмы, притупляя контррегулирующие реакции на гипогликемию у крыс в сознании.Диабет52 : 2198 –2204,2003
- ↵
Сандовал Д.А., Пинг Л., Нил Р.А., Гонг Б., Уолш К., Дэвис С.Н.: Зависящие от области мозга эффекты дексаметазона на контррегуляторные реакции на гипогликемию у крыс в сознании. Am J Physiol Regul Integr Comp Physiol288 : R413 –R419,2005
- ↵
de Galan BE, Rietjens SJ, Tack CJ, Van Der Werf SP, Sweep CGJ, Lenders JWM, Smits P: предшествующий адреналин ослабляет реакцию на контррегуляторные гормоны, но не высвобождает их. при последующей гипогликемии.J Clin Endocrinol Metab88 : 5462 –5467,2003
- ↵
McCall AL, Millington WR, Wurtman RJ: Метаболическое топливо и транспорт аминокислот в мозг при экспериментальном сахарном диабете. Proc Natl Acad Sci U S A79 : 5406 –5410,1982
МакКолл А.Л., Фиксман Л.Б., Флеминг Н., Торнхейм К., Чик В., Рудерман Н.Б .: Хроническая гипогликемия увеличивает транспорт глюкозы в мозге. Am J Physiol Endocrinol Metab251 : E442 –E447,1986
Koranyi L, Bourey RE, James D, Mueckler M, Fiedorek FT Jr, Permutt MA: Экспрессия гена транспортера глюкозы в головном мозге крысы: претрансляционные изменения, связанные с хронической инсулино-индуцированной гипогликемией, голоданием и диабетом .Mol Cell Neurosci2 : 244 –252,1991
Кумагаи А.К., Канг Ю.С., Боадо Р.Дж., Пардридж В.М.: Повышение регуляции гематоэнцефалического барьера, белка транспортера глюкозы GLUT-1 и мРНК при экспериментальной хронической гипогликемии. Диабет44 : 1399 –1404,1995
- ↵
Simpson IA, Appel NM, Hokari M, Oki J, Holman G, Maher F, Koehler-Stec E, Vannucci S, Smith Q: Переносчик глюкозы через гематоэнцефалический барьер: эффекты гипогликемии — и снова о гипергликемии. J Neurochem72 : 238 –247,1999
- ↵
Бойл П.Дж., Надь Р.Дж., О’Коннор А.М., Кемперс С.Ф., Йео Р.А., Куоллс С. Адаптация в потреблении глюкозы в мозге после рецидивирующей гипогликемии.Proc Natl Acad Sci U S A91 : 9352 –9356,1994
- ↵
Бойл П.Дж., Кемперс С.Ф., О’Коннор А.М., Надь Р.Дж.: Поглощение глюкозы мозгом и неосведомленность о гипогликемии у пациентов с инсулинозависимым сахарным диабетом. N Engl J Med333 : 1726 –1731,1995
- ↵
Segel SA, Fanelli CG, Dence CS, Markham J, Videen TO, Paramore DS, Powers WJ, Cryer PE: транспорт глюкозы из крови в мозг, метаболизм глюкозы в мозге и церебральный кровоток не увеличиваются после гипогликемии.Диабет50 : 1911 –1917,2001
- ↵
Bingham EM, Dunn J, Sutcliffe-Goulden J, Marsden P, Amiel S: Влияние неосведомленности о гипогликемии на содержание, транспорт и метаболизм глюкозы в мозге во время эугликемии и гипогликемии у человека (аннотация) . Диабетология47 : A83 , 2004
- ↵
de Vries MG, Arseneau LM, Lawson ME, Beverly JL: Внеклеточная глюкоза в вентромедиальном гипоталамусе крыс во время острой и рецидивирующей гипогликемии. Диабет52 : 2767 –2773,2003
- ↵
McCrimmon R, Jacob RJ, Fan X, McNay EC, Sherwin RS: Влияние повторяющейся предшествующей гипогликемии и хронической гипергликемии на внеклеточные концентрации глюкозы в стволе мозга во время острой гипогликемии у диабетических крыс BB в сознании.Диабетология46 : 1658 –1661,2003
- ↵
McNay EC, Sherwin RS: Влияние повторяющейся гипогликемии на пространственное познание и когнитивный метаболизм у нормальных и диабетических крыс. Диабет53 : 418 –425,2004
- ↵
Criego AB, Tkac I, Kumar A, Gruetter R, Seaquist ER: Концентрация глюкозы в мозге у здоровых людей, подвергающихся рецидивирующей гипогликемии (Резюме). Диабет54 (Приложение 1) : A156 , 2005
- ↵
Criego AB, Tkac I, Kumar A, Thomas W, Gruetter R, Seaquist ER: Концентрации глюкозы в головном мозге у пациентов с диабетом 1 типа и не осознающими гипогликемию.J Neurosci Res79 : 42 –47,2005
- ↵
Seaquist ER, Tkac I, Damberg G, Thomas W, Gruetter R: Концентрации глюкозы в мозге при плохо контролируемом сахарном диабете, измеренные с помощью магнитно-резонансной спектроскопии в сильном поле. Обмен веществ54 : 1008 –1013,2005
- ↵
Мейсон Г.Ф., Петерсен К.Ф., Ротман Д.Л., Шульман Г.И.: Повышенный транспорт и утилизация монокарбоксилатной кислоты мозгом у диабетиков 1 типа во время гипогликемии: возможный механизм незнания гипогликемии (Аннотация).Диабет53 (Приложение 2) : A42 , 2004
- ↵
Routh VH: глюкозочувствительные нейроны вентромедиального ядра гипоталамуса (VMN) и вегетативная недостаточность, связанная с гипогликемией (HAAF). Диабет Metab Res Rev19 : 348 –356,2003
- ↵
Борг В.П., Шервин Р.С., Во время MJ, Борг М.А., Шульман Г.И.: Локальная вентромедиальная глюкопения в гипоталамусе вызывает выброс регулирующих гормонов. Диабет44 : 180 –184,1995
- ↵
Borg MA, Sherwin RS, Borg WP, Tamborlane WV, Shulman GI: Локальная перфузия глюкозы в вентромедиальном гипоталамусе блокирует контррегуляцию во время системной гипогликемии у бодрствующих крыс.J Clin Invest99 : 361 –365,1997
- ↵
ДиРокко Р.Дж., Гриль Х.Дж.: Передний мозг не важен для симпатоадреналовой гипергликемической реакции на глюкопривацию. Наука204 : 112 –114,1979
- ↵
Biggers DW, Myers S, Neal D, Stinson R, Cooper NB, Jaspan JB, Wiliams PE, Cherrington AD, Frizzell RT: Роль мозга в противодействии регуляции инсулино-индуцированной гипогликемии у собак. Сахарный диабет37 : 7 –16,1989
- ↵
Тевес Д., Видин Т.О., Крайер П.Е., Пауэрс В.Дж .: Активация медиальной префронтальной коры головного мозга человека во время вегетативных реакций на гипогликемию.Proc Natl Acad Sci U S A101 : 6217 –6221,2004
- ↵
Данн Дж., Крэнстон И.К., Марсден П.К., Амиэль С.А.: Измерение перфузии мозга в ответ на острую гипогликемию у здоровых добровольцев: исследование позитронно-эмиссионной томографии 15 0 (Аннотация) . Diabetologia47 (Приложение 1) : A322 , 2004
- ↵
Онгур Д., Прайс Дж. Л.: Организация сетей в орбитальной и медиальной префронтальной коре головного мозга крыс, обезьян и людей. Цереб Кортех10 : 206 –219,2000
- ↵
Tkacs NC, Pan Y, Raghupathi R, Dunn-Meynell AA, Levin BE: Кортикальное окрашивание фтор-нефритом и притупление адреномедуллярной реакции на гипогликемию после некомной гипогликемии у крыс.J Cerebr Blood Flow Metab, 2005 г. [Epub перед печатью]
- ↵
Данн-Мейнелл А.А., Раус В.Х., Канг Л., Гасперс Л., Левин Б.Е .: Глюкокиназа является вероятным медиатором чувствительности к глюкозе в центральных нейронах, как возбужденных, так и ингибированных глюкозой. Диабет51 : 2056 –2065,2002
Ян X-J, Kow L-M, Pfaff DW, Mobbs CV: метаболические пути, которые опосредуют ингибирование гипоталамических нейронов глюкозой. Диабет53 : 67 –73,2004
- ↵
Левин Б.Е., Раус В.Х., Канг Л., Сандерс Н.М., Данн-Мейнелл А.А.: Глюкозондирование нейронов.Диабет53 : 2521 –2528,2004
- ↵
Ронсеро I, Альварес Э., Чоуэн И.А., Санс С., Рабано А., Васкес П., Бласкес Э. Экспрессия изоформы переносчика глюкозы GLUT-2 и генов глюкокиназы в мозге человека. J Neurochem88 : 1203 –1210,2004
- ↵
Габриэли I, Шамун H: Фруктоза нормализует специфические контррегуляторные реакции на гипогликемию у пациентов с диабетом 1 типа. Диабет54 : 609 –616,2005
- ↵
McCrimmon RJ, McNay E, Chan O, Fan X, Catherine YW, Sherwin RS: Роль рецептора CRH-2 в вентромедиальном гипоталамусе в модулировании контррегуляторных реакций на гипогликемию (Аннотация).Диабет54 (Приложение 1) : A26 , 2005
- ↵
Sanders NM, Ritter S: Повторное индуцированное 2-дезокси-d-глюкозой глюкопривация ослабляет экспрессию Fos и глюкорегуляторные ответы во время последующей глюкопривации. Диабет49 : 1865 –1874,2000
- ↵
Эван С.Б., Уилкинсон К.В., Гронбек П., Беннетт Дж. Л., Таборски Г. Дж. Мл., Фиглевич Д. П. Инактивация PVN во время гипогликемии частично имитирует вегетативную недостаточность, связанную с гипогликемией. Am J Physiol Regul Integr Comp Physiol284 : R57 –R65,2003
- ↵
Evans ML, McCrimmon RJ, Flanagan DE, Keshavarz T, Fan X, McNay EC, Jacob RJ, Sherwin RS: Гипоталамические АТФ-чувствительные каналы K + играют ключевую роль в обнаружении гипогликемия и запуск контррегуляторных реакций адреналина и глюкагона.Диабет53 : 2542 –2551,2004
- ↵
McCrimmon RJ, Fan X, Evans ML, McNay E, Chan O, Ding Y, Sherwin RS: Каналы VMH K-ATP играют ключевую роль в распознавании гипогликемии и запуске контррегулирующих гормональных реакций ( Абстрактный). Диабет53 (Приложение 2) : A42 , 2004
- ↵
McCrimmon RJ, Fan X, Ding Y, Zhu W., Jacob RJ, Sherwin RS: Возможная роль AMP-активированной протеинкиназы в восприятии гипогликемии в вентромедиальном гипоталамусе. Диабет53 : 1953 –1958,2004
Хан С.-М, Ким М.-С, Намкунг С., Чан П., Чун С., Парк Дж-Й, Ли К-У: Гипоталамическая AMP-активированная протеинкиназа опосредует контррегуляторные реакции на гипогликемию (Аннотация).Диабет54 (Приложение 1) : A387 , 2005
- ↵
McCrimmon RJ, Fan X, Shaw M, Zhu W, Ding Y, Sherwin RS: Обращение дефектных гормональных реакций на гипогликемию посредством активации AMP-киназы в вентромедиальном гипоталамусе крыс (Аннотация). Диабет54 (Приложение 1) : A69 , 2005
- ↵
Джордано Р., Гроттоли С., Бросса П., Пеллегрино М., Дестефанис С., Ланфранко Ф., Джанотти Л., Гиго Е., Арват Е.: Альпразолам (бензодиазепин, активирующий рецептор ГАМК) снижает нейрорецепторные реакции. -индуцированная гипогликемия у человека.Клин Эндокринол59 : 314 –320,2003
- ↵
Чан О, Чжу В., Дин Й., МакКриммон Р.Дж., Шервин Р.С.: Модуляция ГАМК в вентромедиальном гипоталамусе в первую очередь влияет на глюкагон и симпатоадреналовые реакции на гипогликемию (Аннотация). Диабет54 (Приложение 1) : A154 , 2005
- ↵
Mastaitis JW, Wurmbach E, Cheng H, Sealfon SC, Mobbs CV: Острая индукция экспрессии генов в головном мозге и печени инсулино-индуцированной гипогликемией. Диабет54 : 952 –958,2005
- ↵
Томас М., Шервин Р.С., Мерфи Дж., Керр Д.: Важность церебрального кровотока для распознавания и физиологических реакций на гипогликемию.Диабет46 : 829 –833,1997
- ↵
Fisher SJ, Brüning JC, Lannon S, Kahn CR: Передача сигналов инсулина в центральной нервной системе имеет решающее значение для нормального симпатоадреналового ответа на гипогликемию. Диабет54 : 1447 –1451,2005
- ↵
Fisher SJ, Daphna-Iken D, Perez R, Oloruntoba O, Kahn CR: Гипогликемия, зависимая от инсулино-опосредованной вегетативной недостаточности (Аннотация). Диабет54 (Приложение 1) : A70 , 2005
- ↵
Gruetter R: Гликоген: забытый церебральный накопитель энергии.J Neurosci Res74 : 179 –183,2003
- ↵
Cruz NF, Dienel GA: Высокий уровень гликогена в мозге крыс с минимальными воздействиями окружающей среды: влияние на метаболический вклад рабочих астроцитов. J Cereb Blood Flow Metab22 : 1476 –1489,2002
- ↵
Choi I-Y, Seaquist ER, Gruetter R: Влияние гипогликемии на метаболизм гликогена в мозге in vivo. J Neurosci Res72 : 25 –32,2003
- ↵
Oz G, Seaquist ER, Kumar A, Criego AB, Benedict LE, Rao JP, Gruetter R: неинвазивное измерение содержания гликогена в мозге человека (аннотация).Диабет54 (Приложение 1) : A158 , 2005
- ↵
Choi IY, Tkác̆ I, Uğurbil K, Gruetter R: неинвазивные измерения [1- 13 C] концентраций и метаболизма гликогена в мозге крысы in vivo. J Neurochem73 : 1300 –1308,1999
- ↵
Галассетти П., Манн С., Тейт Д., Нил Р.А., Коста Ф., Вассерман Д.Х., Дэвис С.Н.: Влияние предшествующих длительных упражнений на последующие контррегулирующие реакции на гипогликемию. Am J Physiol280 : E908 –E917,2001
- ↵
МакГрегор В.П., Грейве Дж. С., Банарер С., Крайер П. Е.: Ограниченное влияние интенсивных упражнений на защиту от гипогликемии: актуальность для вегетативной недостаточности, связанной с гипогликемией.Диабет51 : 1485 –1492,2002
- ↵
Jones TW, Porter P, Sherwin RS, Davis EA, O’Leary P, Frazer F, Byrne G, Stick S, Tamborlane WV: Снижение реакции эпинефрина на гипогликемию во время сна. N Engl J Med338 : 1657 –1662,1998
- ↵
Банарер С., Крайер П.Е. Вегетативная недостаточность, связанная со сном, связанная с гипогликемией, при диабете 1 типа: уменьшение пробуждения ото сна во время гипогликемии. Диабет52 : 1195 –1203,2003
- ↵
Шин Х-В, Бан Й-Дж, Ли Х-В, Лим Х-Дж, Юн С.-М, Чанг С.-Х: возбуждение от внутривенного введения эпинефрина зависит от глубины анестезии.Can J Anesth51 : 880 –885,2004
- ↵
Крайер PE, Дэвис С.Н., Шамун H: Гипогликемия при диабете. Уход за диабетом26 : 1902 –1912,2003
- ↵
Болли ГБ: Лечение и профилактика гипогликемии и ее незнания при диабете 1 типа. Rev Endocr Metab Disord4 : 335 –341,2003
Реакция надпочечников при стрессовых ситуациях и усталости надпочечников
Надпочечники реагируют на серьезный стресс из любого источника, активируя систему «бей или беги».Ответственные гормоны — норадреналин и адреналин (также называемый адреналином).
Когда стрессор распознается, ось гипоталамус-гипофиз-надпочечники (HPA) приводится в движение. В конце этого потока гормонов надпочечники высвобождают кортизол, борясь с последствиями стресса. Адреномедуллярная гормональная система (АГС) может активироваться при сильном стрессе. Мозговое вещество надпочечников вырабатывает адреналин, давая организму дополнительный заряд энергии как часть реакции борьбы или бегства.
Когда напряжение уменьшается, активируется противоположная система. AHS отдыхает, и ось HPA возвращается к нормальной работе. Это ответ «отдыхай и переваривай». Эта система в первую очередь регулируется парасимпатической нервной системой или ПНС. С помощью этой системы тело расслабляется, любой оставшийся адреналин метаболизируется, и организм восстанавливается после стресса.
Реакция надпочечников и утомление надпочечников
Когда надпочечники подвергаются постоянной бомбардировке стрессовых факторов, потребность в кортизоле и других гормонах стресса становится слишком большой.В конечном итоге надпочечники теряют способность секретировать достаточное количество этих гормонов.
Когда стресс продолжается, как это часто бывает в нашем мире, AHS остается активированным. Организм больше не может эффективно модулировать ПНС, чтобы оправиться от последствий стресса.
Это указывает на истощение надпочечников, продвинутую стадию состояния, известного как синдром усталости надпочечников (AFS). На данный момент тело находится в беспорядке, доступные только ограниченные ресурсы и способность надпочечников.Он решает, что лучший вариант — убежать от всего, что его напрягает. Это приводит к тому, что AHS продолжает выделять адреналин или адреналин, чтобы подготовить организм к бегству.
Адреналин — мощный гормон, поражающий многие части тела. Норэпинефрин — это нейротрансмиттер, который действует локально, воздействуя на определенные органы, такие как мозг, чтобы вы были более внимательными. Норэпинефрин также попадает в сердце и заставляет сердце биться сильнее. Некоторые люди симптоматически сообщают, что их сердце бьется сильнее, чем обычно.Оба эти вещества активируют различные части тела, заставляя их убегать от угроз. Адреналин намного сильнее норадреналина. Некоторые из них необходимы для повседневной жизни. Например, без норэпинефрина встать становится проблематично. Баланс между кортизолом, норадреналином и адреналином имеет решающее значение для хорошего самочувствия, особенно в условиях стресса.
К сожалению, адреналин — это гормон, у которого нет гормонов, нейтрализующих его. Он вызывает выброс большего количества адреналина, и, таким образом, создается положительная обратная связь.В конечном итоге это может привести к нисходящему каскаду нестабильности, который, если его не остановить, закончится коллапсом.
Реактивный симпатоадреналовый ответ (RSR)
Когда организм находится в фазе 3 усталости надпочечников и стресса, симпатоадреналовая система (САС) наращивает свою активность. SAS отвечает за активацию и инактивацию надпочечников, а также за высвобождение норадреналина и адреналина.
Это вызывает автоматическую серию реакций организма, называемых реактивной симпатоадреналовой реакцией (RSR) , которые наполняют тело адреналином.Напротив, реактивный симпатический обертон (RSO) указывает на перегрузку норадреналина. Есть существенные отличия. RSO немного менее интенсивен, чем RSR. При RSO может ощущаться учащенное сердцебиение, но частота пульса нормальная. RSR, с другой стороны, может вызвать тахикардию, ЖЭ и фибрилляцию предсердий, если она чрезмерная.
Часто RSR и RSO смешиваются друг с другом. Оба присутствуют чрезмерно с неослабевающим стрессом. Начинается множество иногда субклинических симптомов.Они могут включать реакцию надпочечников, ощущение головокружения, изменчивое кровяное давление, нерегулярный пульс, непереносимость холода и жары, головокружение, потоотделение, паническую атаку, постуральную ортостатическую тахикардию и обмороки. Некоторые из этих симптомов вызывают чрезмерное количество адреналина и норэпинефрина. Другие могут быть вызваны дисбалансом двух химических веществ.Эта фаза представляет собой стадию утомления надпочечников, когда требуется тщательное обследование в течение определенного периода времени для точной оценки состояния.Многие врачи видят лишь «снимок» симптомов пациента, упуская из виду первопричину. В первую очередь основное внимание уделяется сердцу, поскольку нерегулярная частота сердечных сокращений часто является первой клинической жалобой, с которой больной обращается к врачу. Кардиологическое обследование всегда в норме, и пациентам советуют пойти домой и «расслабиться». Из-за иногда неопределенной природы симптомов AFS некоторые врачи не принимают во внимание их все. Что нужно, так это больше «видео», чем «снимок», охватывающий симптомы пациента во времени.
RSR и усталость надпочечников
Традиционно обученным врачам обычно дают узкую картину совокупности симптомов реакции надпочечников, обращаясь только к одному симптому или одной системе органов, которая, по-видимому, наиболее поражена. Необходима более полная точка зрения. При этом необходимо учитывать все системы организма и то, как они взаимосвязаны.
Эта точка зрения называется моделью стресс-реакции NeuroEndoMetabolic (NEM). Используя модель NEM, практикующие врачи рассматривают всю картину симптомов, включая несколько посещений с течением времени. Требуется терпение.
Особенно в фазе 3 AFS, когда происходит RSR, организм становится сенсибилизированным практически к любому раздражителю, который может стать источником стресса. Событие, на которое обычно не обращали внимания, может запустить каскад телесных реакций, которые вернут человека в болото необычайно высоких уровней адреналина и норадреналина, вызывая поток симптомов, описанных выше.
Это наводнение может быть вызвано такими простыми и обычными действиями, как поедание обильной еды, полной углеводов, жаркий спор, просмотр боевика, питье очень холодной воды, длительное пребывание на солнце, долгая работа перед компьютер, употребление в пищу трудно перевариваемой пищи или длительная тяжелая прогулка.
При активации RSR обычно точный баланс тела нарушается, потому что симпатоадреналовая система направляет больше крови в мозг, чтобы обеспечить выживание тела.Это может привести к резким колебаниям в метаболической и гормональной системах. Это приводит к острой слабости надпочечников и называется срывом надпочечников. Симптомы, обычно наблюдаемые при AFS, в этих условиях усиливаются. Время на восстановление после такого краха может быть значительно больше, в зависимости от степени слабости надпочечников.
Стрессоры, которые могут повлиять на RSR
Стрессоры не обязательно должны быть физическими, чтобы активировать RSR и реакцию надпочечников. Одно исследование показало, что психологический стресс может привести к активации АГЧ, что повысит риск сердечно-сосудистых заболеваний.Это происходит потому, что выброс адреналина и норадреналина в сочетании с продолжающимся психологическим стрессом может повысить риск сердечно-сосудистых заболеваний. Это очевидно в профессиях, где стресс — это укоренившийся компонент.
У пациентов с гипогликемией SAS может служить системой раннего предупреждения для организма. К сожалению, также возможно, что SAS может стать неэффективным в этом отношении. Если вы испытаете это, у вас более высокий риск проблем с центральной нервной системой из-за низкого уровня сахара в крови.SAS, кажется, играет роль в определении уровня глюкозы в крови.Многократное воздействие метаболического стресса, вызванного гипогликемией, по-видимому, снижает реакцию САС. Это может быть связано с частью мозга, которая называется задним паравентрикулярным ядром таламуса. Эта структура, по-видимому, модулирует реакцию центральной нервной системы на продолжающийся стресс, как и в AFS.
Исследования также показали, что количество катехоламинов в крови, таких как адреналин и норадреналин, может предсказывать повышение артериального давления в течение 18 лет после всплеска этих химических веществ.Это открытие может иметь значение для развития гипертонической болезни независимо от исходного артериального давления.
Решение проблем с надпочечниками
При поиске способов справиться с нарушениями функции надпочечников, наблюдаемыми при использовании RSR и AFS в целом, важно найти специалиста в области здравоохранения, имеющего подготовку и навыки, необходимые для адекватной оценки и решения. В первую очередь следует дать профессионалу достаточно времени для точной оценки реакции надпочечников.После того, как усилия по разрешению проблем начались, процесс требует времени. Возможно, наиболее важным соображением является строгое соблюдение режима, предписанного практикующим врачом.
Могут быть рекомендованы лекарства, например бета-блокаторы, для контроля частоты сердечных сокращений. Это часто может иметь краткосрочную пользу, но в долгосрочной перспективе может быть очень проблематично. Рекомендуется соблюдать осторожность.
Снижение стресса — первый шаг после оценки. Напряжение является решающим фактором в возникновении как AFS, так и результирующих RSR и RSO.Эта постоянная реакция надпочечников лишает организм возможности справляться со стрессом.
Любой стресс может вызвать симптомы, описанные выше. Если можно определить источник стресса в вашей жизни, сделайте все необходимое, чтобы уменьшить его. Если вы не уверены в стрессе в своей жизни, примите меры, чтобы расслабиться и устранить все возможные факторы стресса. Ясно, что вы не можете исключить из своей жизни все факторы стресса, но важно внести необходимые изменения, чтобы удалить как можно больше факторов.
Одно изменение, которое вы можете сделать, — это вложить в свою жизнь как можно больше позитива. Положительные мысли, положительные высказывания и положительные люди могут уменьшить некоторые негативные факторы, усугубляющие стресс.
Во-вторых, внесите изменения в свой рацион. Пища, которую вы едите, влияет не только на ваше физическое тело, но и на ваши эмоции. Исключите продукты, которые вызывают воспаление и токсины в организме. Исследования показывают, что воспаление является причиной все большего числа физических проблем, с которыми люди сталкиваются.Большинство людей не знают о токсинах, которые они приносят в свой организм через пищу, которую они едят, и окружающую среду, в которой они живут и работают. Как при AFS, так и при RSR функция печени также может быть нарушена. Печень — один из основных органов детоксикации вашего тела.
Одним из основных токсинов является кофеин. Сокращение употребления кофе, чая и шоколада может снизить количество кофеина в организме. Кофеин затрудняет сон, поэтому сон необходим для восстановления после стресса.Сахар во многих формах также является токсином для вашего тела.Кукурузный сироп с высоким содержанием фруктозы и искусственные подсластители особенно токсичны. Эти вещества могут вызывать реакцию надпочечников, усиливая воспаление в организме и потенциально приводя к серьезным заболеваниям, таким как диабет 2 типа.
Приготовление и обработка продуктов в микроволновой печи лишает их питательных веществ, в которых нуждается ваше тело. Были признаки того, что некоторые продукты, приготовленные в микроволновой печи, также производят канцерогены. Добавленные в пищу наполнители и консерванты также не усваиваются организмом, что приводит к значительной потере энергии, необходимой во время попытки пищеварения.
Вы также можете добавить в свой рацион продукты и добавки, чтобы изменить ситуацию к лучшему.
Добавки и травы , такие как священный базилик, магний, витамины B12, B5, D3 и C, ашваганда, цинк и рыбий жир, полезны с точки зрения питания. К сожалению, они также могут быть слишком стимулирующими для организма, когда оно уже находится в состоянии перегрузки. Возможно, вам придется быть особенно осторожным с травами и железами, включая ашвагандху. В некоторых случаях симптомы могут ухудшиться. Если вы можете получить эти вещества из продуктов, это лучший источник.Если нет, их можно принимать в качестве добавок.
Заключение
Если вы испытываете симптомы реакции надпочечников, описанные в этой статье, обязательно проконсультируйтесь с хорошо обученным практикующим врачом. Будьте готовы выслушать рекомендации своего врача и дать ему достаточно времени для работы. Вы можете изменить свое здоровье. Все, что вам нужно сделать, это сделать правильный выбор.
Кризис гипертонии в хирургии надпочечников и лечение послеоперационной гипотензии — Польский хирургический журнал — Том 82, выпуск 4 (2010) — PSJD
Кризис гипертонии в хирургии надпочечников и лечение послеоперационной гипотензии — Польский хирургический журнал — Том 82, выпуск 4 ( 2010) — ПСЖД — ЯддаEN
Целью исследования было представить наш опыт лечения феохромоцитомы, которая может иметь нетипичные проявления или их полное отсутствие.Хирургия по-прежнему остается основным лечением. С внедрением малоинвазивного метода хирургический выбор между открытым и видеоскопическим остается неизменным. Правильная диагностика, подготовка и хирургическое лечение позволяют избежать серьезных сердечно-сосудистых осложнений. При лечении важными вопросами являются предоперационный или интраоперационный гипертонический криз и гипотония, возникающая после удаления опухоли. На основании нашего исследования с 29.10.1997 по 31.01.2009 авторы показывают способы и принципы подготовки, а также интра- и послеоперационные осложнения, связанные с проведенной операцией.Дополнительно обсуждается проблема феохромоцитом, клинически бессимптомных, так называемых тихих феохромоцитом. Оцениваемый материал — 125 пациентов с феохромоцитомой. 32 (25,6%) прооперированы открытым классическим методом, 93 (74,4%) — лапароскопическим способом из латерального трансперитонеального доступа. Выводы. 1. Течение и результат хирургического лечения феохромоцитомы зависят от правильной диагностики и предоперационной подготовки. 2. Лапароскопическая адреналэктомия из латерального трансперитонеального доступа должна рассматриваться как референтная операция в лечении феохромоцитомы.3. Клинически бессимптомная феохромоцитома требует обычной подготовки, как и другие формы феохромоцитомы.
- Отделение общей, сосудистой и трансплантологической хирургии, Варшавский медицинский университет
- Отделение общей, сосудистой и трансплантологической хирургии, Варшавский медицинский университет
- Отделение гипертонии, Институт кардиологии, Варшава
- Отделение гипертонии, Институт кардиологии, Варшава
- II отделение анестезиологии и интенсивной терапии Варшавского медицинского университета
- Отделение эндокринологии, Центр последипломного медицинского образования, Варшава
- Отделение эндокринологии, Центр последипломного медицинского образования, Варшава
- Отделение общей, сосудистой и трансплантологической хирургии, Варшавский медицинский университет
- Grupa Robocza Polskiego Towarzystwa Nadciśnienia Tętniczego: Wytyczne dotyczące diagnostyki i leczenia chorych z guzem chromochłonnym.Nadciśnienie Tętnicze 2006; 10: 1-19.
- Eisenhofer G: Феохромоцитома: последние достижения и лежачие полицейские на пути к дальнейшему прогрессу. J Hypertens 2006; 24: 2341-42. [Crossref] .
- Sardesai SH, Mourant AJ, Sivathandon Y et al .: Кардиомиопатия, вызванная феохромоцитомой и катехоламином, проявляющаяся в виде сердечной недостаточности. Br Heart J 1990; 63: 234-37.
- Отто М: Operacyjne leczenie guzów nadnerczy. W: Янушевич А, Щепаньска-Садовская Э, Снайдерман М (красный.) Nadciśnienie Tętnicze. Medycyna Praktyczna; Краков 2007, с. 849-859.
- Микколли П., Рафаэлли М., Берти П. и др.: Хирургия надпочечников до и после введения лапароскопической адреналэктомии. Br J Surg 2002; 89: 779-82.
- Брауэрс Ф.М., Сендерс Дж. В., Эйзенхофер Г. и др.: Феохромоцитома как неотложная эндокринная проблема. Rev Endocr Metab Disord 2003; 4: 121-28.
- Prys-Roberts C Феохромоцитома — недавний прогресс в ее лечении.Br J Anaesth 2000; 85: 44-57.
- Шен С.Дж .: Периоперационный гипертонический криз при клинически бессимптомных феохромоцитомах: отчет о четырех случаях. Chang Gung Med J 2005; 28: 44-50.
- Райш Н., Пенчковская М., Янушевич А. и др .: Феохромоцитома: проявление, диагностика и лечение. J Hypertens 2006; 24: 2331-39. [Crossref] .
- Вербель С.С., Обер К.П .: Феохромоцитома. Обновленная информация о диагностике, локализации и лечении. Med Clin North Am 1995; 79: 131-53.
- Гольдштейн Р. Э., О’Нил Дж. А., Холкомб Г. В. Клинический опыт лечения феохромоцитомой более 48 лет. Ann Surg 1999; 229: 755-766.
- Lenders JWM, Eisenhofer G, Mannelli M et al .: Феохромоцитома. Lancet 2005; 366: 665-75.
- Manger WM, Eisehofer G: Феохромоцитома: обновление диагностики и лечения. Curr Hypertens Rep 2004; 6: 477-84.
- Ньюэлл К.А., Принц Р.А., Пиклман Дж. И др.: Мультисистемный кризис феохромоцитомы.Неотложная хирургическая помощь. Arch Surg 1988; 123: 956-59.
- Миядзима А., Накашима Дж., Баба С. и др .: Случайно обнаруженная феохромоцитома. J Urol 1997; 157: 1566-68.
- Браво Э.Л .: Феохромоцитома: новые концепции и тенденции будущего. Kidney Int 1991; 40: 544-51. [Crossref]
- Ньюэлл К.А., Принц Р.А., Брукс М.Х. и др.: Изменения плазменных катехоламинов во время удаления феохромоцитомы. Хирургия 1988; 104: 1064-71.
- Boutros AR, Bravo E, Zanettin G et al.: Периоперационное ведение 63 пациентов с феохромоцитомой. Cleve Clin J. Med, 1990; 57: 613-19.
- Гросс, доктор медицины, Шапиро Б.: Клинический обзор 50: клинически бессимптомные образования надпочечников. J Clin Endocr Metab 1993; 77: 885-94.
- Крейн Н.К.: Феохромоцитома без подозрений. Arch Intern Med 1986; 146: 54-62.
- Lucon Am, Pereira MA, Mendonca BB и др .: Феохромоцитома: исследование 50 случаев. J Urol 1997; 157: 1208-12.
- Neumann HPH, Berger DP, Sigmund G et al.: Феохромоцитомы, множественная эндокринная неоплазия 2 типа и болезнь фон Гиппеля-Линдау. N Engl J Med 1993; 329: 1531-38.
- Пакак К., Илиас I, Адамс К.Т. и др.: Биохимическая диагностика, локализация и лечение феохромоцитомы: основное внимание уделяется множественной эндокринной неоплазии 2 типа по отношению к другим наследственным синдромам и спорадическим формам опухоли. J Int Med 2005; 257: 60-68.
- Ulchaker JC, Goldfarb DA, Bravo EL и др .: Успешные результаты хирургии феохромоцитомы в современную эпоху.J Urol 1999; 161: 764-67.
- Маккензи И.С., Браун М.Дж.: Псевдофеохромоцитома. J Hypertens 2007; 25: 2204-06. [Crossref] [PubMed]
- Sharabi Y, Goldstein DS, Bentho O et al .: Симпато-адреналовая функция у пациентов с пароксизмальной гипертензией — псевдофеохромоцитомой. J Hypertens 2007; 25: 2286-95. [Crossref] [WoS]
- Амос AM, Мак-Робертс JW: синдром Кушинга, связанный с феохромоцитомой. Урология 1998; 52: 331-35. [Crossref]
- Тан Г. Х., Карни Дж. А., Грант С. С. и др.: Сосуществование двусторонней феохромоцитомы надпочечников и идиопатического гиперальдостеронизма. Clin Endocrinol 1996; 44: 606-09.
- Кальцас Г.А., Пападогиас Д., Гроссман А.Б.: Клинические проявления (симптомы и признаки) спорадических и семейных хромаффинно-клеточных опухолей (феохромоцитомы и параганглиомы). W: Ленерт Х. (ред.) Феохромоцитома, патофизиология и клиническое ведение. Front Horm Res Basel, Karger 2004; с.61-75.
- Diner EK, Franks ME, Behari A. et al.: Частичная адреналэктомия: опыт Национального института рака. Урология 2005; 66: 19-23.
- Вальтер М.М., Херринг Дж., Чойк П. и др.: Лапароскопическая частичная адреналэктомия у пациентов с наследственными формами феохромоцитомы. J Urolog 2000; 164: 14-17.
- Walz MK: Степень адреналэктомии при новообразовании надпочечников: щадящая (субтотальная) по сравнению с тотальной адреналэктомией. Surg Clin N Am 2004; 84: 743-53.
- Sturgeon C, Kebebew E: Лапароскопическая адреналэктомия при злокачественных новообразованиях.Surg Clin N Am 2004; 84: 755-74.
Номер заказа на публикацию
bwmeta1.element.-psjd-doi-10_2478_v10035-010-0028-7
В вашем браузере отключен JavaScript.Включите его, чтобы воспользоваться всеми преимуществами этого сайта, а затем обновите страницу.Надпочечниковая недостаточность (болезнь Аддисона) | Johns Hopkins Medicine
Надпочечниковая недостаточность возникает, когда надпочечники не вырабатывают достаточного количества гормона кортизола. У вас два надпочечника. Они расположены чуть выше почек. Они работают с гипоталамусом и гипофизом головного мозга. Кортизол помогает расщеплять жиры, белки и углеводы в организме. Он также контролирует кровяное давление и влияет на работу вашей иммунной системы.
Надпочечниковая недостаточность может быть первичной или вторичной:
Первичная надпочечниковая недостаточность. Это известно как болезнь Аддисона. Возникает при поражении надпочечников. Они не вырабатывают достаточного количества гормонов кортизола и альдостерона. Это состояние встречается редко. Это может произойти в любом возрасте.
Вторичная надпочечниковая недостаточность. Это начинается, когда гипофиз не вырабатывает достаточно гормона АКТГ (адренокортикотропина).В результате надпочечники не вырабатывают достаточно кортизола.
Что вызывает надпочечниковую недостаточность?
Первичная надпочечниковая недостаточность чаще всего возникает, когда иммунная система по ошибке атакует здоровые надпочечники. Другие причины могут включать:
Недостаток гормона АКТГ приводит к вторичной надпочечниковой недостаточности. Это может произойти, если вы должны принимать определенные стероиды в течение длительного времени из-за проблем со здоровьем. Например, людям с астмой или ревматоидным артритом может потребоваться прием преднизона.Другие причины включают:
Опухоли гипофиза
Нарушение кровотока в гипофизе
Гипофиз удален или у вас лучевая терапия гипофиза
Части гипоталамуса удалены
Какие симптомы надпочечниковой недостаточности?
При физическом стрессе у вас могут быть легкие симптомы.Симптомы у каждого человека будут разными. Симптомы могут включать:
Слабость
Усталость
Головокружение
Темная кожа (только болезнь Аддисона)
Голубовато-черный цвет вокруг сосков, рта, прямой кишки, мошонки или влагалища (только при болезни Аддисона)
Похудание
Потеря жидкости (обезвоживание)
Отсутствие аппетита
Мышечные боли
Расстройство желудка (тошнота)
Рвота
Диарея
Низкое артериальное давление
Низкий уровень сахара
У женщин с нерегулярными менструациями или без менструаций
Если не лечить, недостаточность надпочечников может привести к:
Эти симптомы могут быть похожи на другие проблемы со здоровьем.Всегда обращайтесь к своему врачу за диагнозом.
Как диагностируется надпочечниковая недостаточность?
Ваш лечащий врач спросит о вашей истории болезни. Вам также понадобится экзамен. Тесты, которые могут диагностировать надпочечниковую недостаточность, включают:
Анализы крови и мочи. Они могут проверять уровни гормонов надпочечников и АКТГ.
Визуальные тесты. К ним относятся рентген, ультразвук и МРТ.
Как лечится надпочечниковая недостаточность?
Ваш лечащий врач подберет для вас лучшее лечение на основе:
Ваш возраст, общее состояние здоровья и прошлое состояние здоровья
Как вы больны
Насколько хорошо вы справляетесь с некоторыми лекарствами, процедурами или терапией
Ожидаемый срок действия состояния
Ваше мнение или предпочтение
Вам нужно будет принимать гормоны, чтобы заменить те, которые не производятся надпочечниками.В основном это кортизол. Но если у вас болезнь Аддисона, вам может потребоваться также альдостерон.
Болезнь Аддисона может быть смертельной. Лечение часто начинается с внутривенного введения жидкостей и лекарств, называемых кортикостероидами. Вы можете принимать эти лекарства внутрь или внутривенно. Возможно, вам придется принимать их до конца жизни. Возможно, вам также понадобится принимать другие лекарства (флудрокортизоны). Это может помочь поддерживать нормальный уровень натрия и калия в организме.
Какие осложнения при надпочечниковой недостаточности?
У вас могут появиться внезапные тяжелые симптомы.Это называется острой надпочечниковой недостаточностью или аддисонским кризом. Это может произойти, когда ваше тело подвергается стрессу. Это может произойти по многим причинам, таким как болезнь, лихорадка, операция или обезвоживание. У вас также может быть кризис, если вы перестанете принимать стероиды или резко снизите количество стероидов. Симптомы аддисонского криза включают симптомы надпочечниковой недостаточности или болезни Аддисона. Но если аддисоновский кризис не лечить, он может привести к:
Жизнь с надпочечниковой недостаточностью
Принимайте лекарство точно в соответствии с предписаниями.Вы также должны всегда иметь при себе карточку или бирку медицинского предупреждения. Это поможет вам получить надлежащее лечение в случае возникновения чрезвычайной ситуации. Во время путешествий всегда имейте при себе аптечку с уколом кортизола.
Когда мне следует позвонить своему врачу?
Любое состояние, вызывающее стресс для вашего тела, может повлиять на количество необходимых вам лекарств. Позвоните своему врачу, если:
У вас есть какое-либо заболевание, особенно высокая температура, рвота или диарея
Вы забеременели
Вам нужна операция
Немедленно обратитесь за медицинской помощью, если у вас возникли внезапные тяжелые симптомы (аддисонский криз).
Основные сведения о надпочечниковой недостаточности (болезнь Аддисона)
Надпочечниковая недостаточность возникает, когда надпочечники не вырабатывают достаточного количества гормона кортизола.





 Возможно, у больных паническим расстройством изменены содержания связанного с серотонином белка тромбоцитов. Также проводились исследования о связи панического расстройства с выработкой антител к серотонину. Имеет значение взаимодействие серотонинергической и других нейромедиаторных систем. Связь между серотонинергической и норадреналинергической системами позволяют объяснить нарушение вегетативной регуляции при паническом расстройстве. СИОЗС могут также уменьшать симптомы панического расстройства опосредованно, через влияние на норадренергическую систему. Например, флуоксетин способен нормализовать MHPG-реакцию на введение клонидина у больных с паническим расстройством.
Возможно, у больных паническим расстройством изменены содержания связанного с серотонином белка тромбоцитов. Также проводились исследования о связи панического расстройства с выработкой антител к серотонину. Имеет значение взаимодействие серотонинергической и других нейромедиаторных систем. Связь между серотонинергической и норадреналинергической системами позволяют объяснить нарушение вегетативной регуляции при паническом расстройстве. СИОЗС могут также уменьшать симптомы панического расстройства опосредованно, через влияние на норадренергическую систему. Например, флуоксетин способен нормализовать MHPG-реакцию на введение клонидина у больных с паническим расстройством. Остальные проявления данная модель связывает с нарушениями функционирования других отделов мозга — лимбические структуры — тревога ожидания, нарушения в префронтальной коре — ограничительное поведение.
Остальные проявления данная модель связывает с нарушениями функционирования других отделов мозга — лимбические структуры — тревога ожидания, нарушения в префронтальной коре — ограничительное поведение.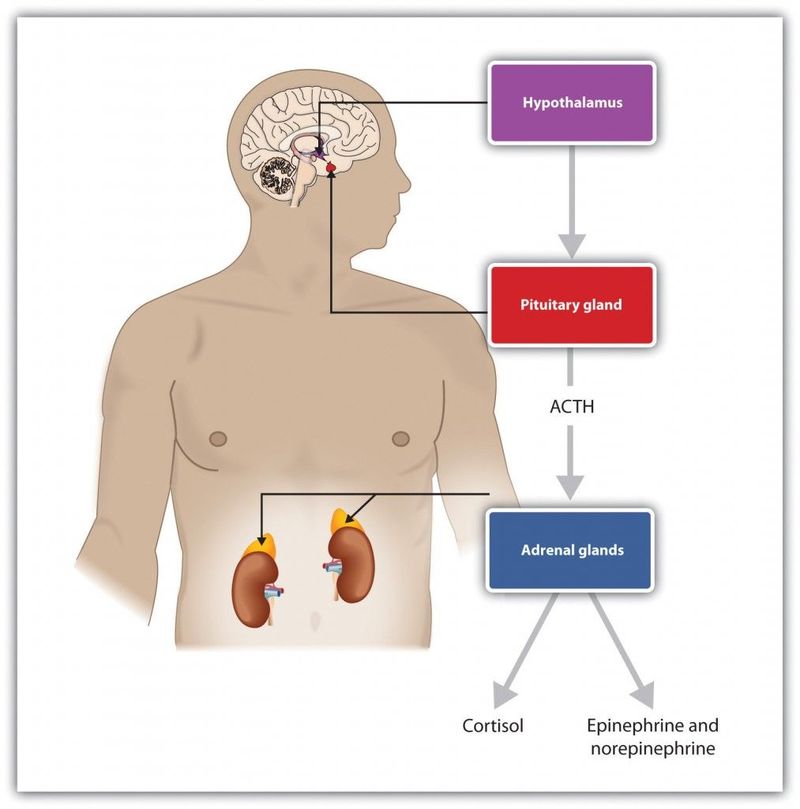 При успешном лечении панического расстройства происходит восстановление нормальной реакции в виде снижения MHPG в ответ на введение клонидина.
При успешном лечении панического расстройства происходит восстановление нормальной реакции в виде снижения MHPG в ответ на введение клонидина.